


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
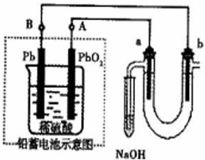 用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)
用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)| A、铅蓄电池负极的反应式为:Pb-2e-=Pb2+ |
| B、铅蓄电池放电时,B极质量减轻,A极质量增加 |
| C、铅蓄电池充电时,A极应与外电源负极相连 |
| D、电解苦卤水时,a电极首先放电的是Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 强电解质 | Fe | NaCl | BaSO4 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H2CO3 | Fe(OH)3 |
| 非电解质 | 蔗糖 | CaCO3 | C2H5OH | H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、加入NaOH溶液并加热,能产生使湿润红色石蕊试纸变蓝的气体,则一定含有N
| ||
| B、将SO2通入溴水,溴水褪色,说明SO2具有漂白性 | ||
| C、某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- | ||
| D、在含FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热除去过量的Cl2,即可得到较纯净的FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、肯定存在的只有KOH和AgNO3 |
| B、NH4Cl、AlCl3肯定不存在 |
| C、KOH和AlCl3可能存在 |
| D、肯定存在的只有NH4Cl、KOH和AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
| A、NH4+:气体法 |
| B、SO42-:沉淀法 |
| C、H+:显色法 |
| D、Cl-:气体法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的离子积变大、pH变小、呈酸性 |
| B、水的离了积不变、pH不变、呈中性 |
| C、水的离子积变小、pH变大、呈碱性 |
| D、水的离子积变大、pH变小、呈中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com