
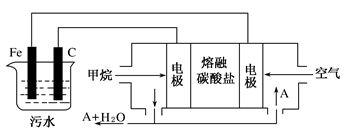
| A.BaSO4 | B.CH3CH2OH | C.Na2SO4 | D.NaOH |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:不详 题型:单选题
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
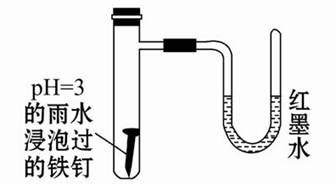
| A.开始时发生的是析氢腐蚀 |
| B.一段时间后发生的是吸氧腐蚀 |
| C.两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+ |
| D.析氢腐蚀的总反应式为2Fe+O2+2H2O=2Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
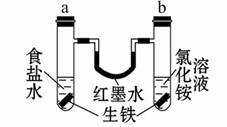
| A.a中发生了吸氧腐蚀,b中发生了析氢腐蚀 |
| B.两试管中负极反应均是:Fe-2e-=Fe2+ |
| C.生铁块中碳作原电池正极 |
| D.在一段时间后,红墨水两边液面变为左低右高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
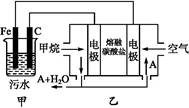
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
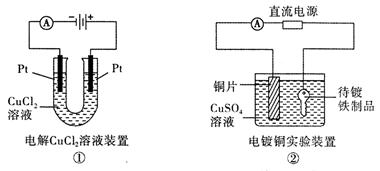
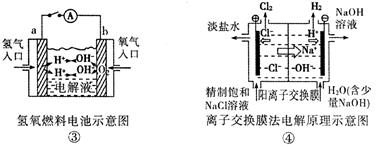
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③闭合电键后,外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Fe2+ + I2设计成如下图所示的原电池
2Fe2+ + I2设计成如下图所示的原电池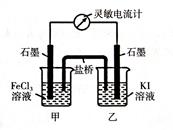
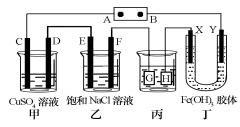
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
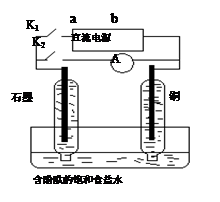
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl— Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,电子沿“b →Cu→电解质溶液→石墨→a”的路径流动 |
| C.断开K2,闭合K1时,铜电极附近溶液变红 |
| D.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl— |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com