
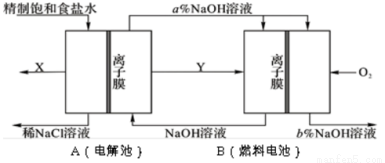
氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2017届辽宁省六校协作体高三上学期期中化学试卷(解析版) 题型:填空题
(1)一个12C原子质量为ag, 有一种X原子的质量为bg.设NA为阿伏伽德罗常数,则X的相对原子质量可表示为:
(2)现有下列物质:①氢氧化钾固体 ②稀硫酸 ③铜片 ④蔗糖 (C12H22O11) 固体 ⑤熔融的氯化钠。
用以上物质的序号填空:属于电解质的是_______________,属于非电解质的是____________;所给状态下能够导电的是______________。
(3)反应(未配平):BrF3+H2O-Br2 +O2+HBrO3+HF已知生成物中Br2与O2的物质的量之比为1:1。则:
+O2+HBrO3+HF已知生成物中Br2与O2的物质的量之比为1:1。则:
①配平后H2O 与HF物质的量之比为 ;
②还原剂为 ;
③如有5molH2O参加反应则参加氧化还原反应的H2O物质的量为 mol
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有200 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液, 产生沉淀的量与所加NaOH溶液的体积的关系如下图所示。则原H2SO4物质的量浓度是( )

A.1mol/L B.2mol/L C.3mol/L D.4mol/L
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
下列各组物质稀溶液相互反应.无论前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
A.Na2CO3溶液与HCl溶液 B.AlCl3溶液与NaOH溶液
C.KAlO2溶液与HCl溶液 D.Na2SiO3溶液与HCl溶液
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三上第一次诊断化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 的溶液中:K+、NH4+、SO42-、NO3-
的溶液中:K+、NH4+、SO42-、NO3-
B.0.1 mol/L NaAlO2溶液:Fe3+ 、H+、Cl-、SO42-
C.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
D.使甲基橙试液显黄色的溶液:Fe2+、Mg2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
研究人员发现了一种“水”电池,其总反应为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。如图用“水”电池为电源电解NaCl溶液的实验中,X电极上有无色气体逸出。下列有关分析正确的是( )
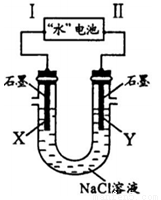
A.I为负极,其电极反应式为Ag+Cl-+e-=AgCl
B.“水”电池内Na+不断向负极作定向移动
C.每转移1mole-,U型管中消耗0.5molH2O
D.“水”电池内,每生成1molNa2Mn5O10,X电极上生成1mol气体
查看答案和解析>>
科目:高中化学 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:选择题
下列化学符号正确的是( )
A.二氧化硅的结构式O=Si=O
B.聚乙烯的结构简式
C.过氧化钠的电子式
D.羟基的电子式
查看答案和解析>>
科目:高中化学 来源:2017届山东省栖霞市高三上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A. 硫离子的结构示意图为
B. 核外电子排布相同的微粒化学性质也相同
C. 氢弹中用到的2H、3H互为同位素
D. 同种元素的原子均有相同的质子数和中子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com