
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有200 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液, 产生沉淀的量与所加NaOH溶液的体积的关系如下图所示。则原H2SO4物质的量浓度是( )

A.1mol/L B.2mol/L C.3mol/L D.4mol/L
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三上统一考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述正确的是( )
①lmolCH3CH2C(CH3)3所含甲基个数为4NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol·L﹣1CH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA
⑥常温常压下,17g甲基(一14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C﹣Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳一碳共价键数目为14NA.
A.①③⑤⑦ B.②③⑥⑧
C.①②④⑧ D.①②⑥⑧
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省六校协作体高三上学期期中化学试卷(解析版) 题型:选择题
16O和18O是氧元素的两种核素,NA表示阿伏伽德罗常数,下列说法正确的是
A. 16O与18O互为同素异形体
B. 16O与18O核外电子排布方式不同
C. 通过化学变化可以实现16O2与18O3间的相互转化
D. 标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三10月月考化学卷(解析版) 题型:选择题
下列关于溶液 浓度说法正确的是( )
浓度说法正确的是( )
A.定容时俯视容量瓶颈刻度线,配得溶液浓度偏低
B.将5.85g NaCl固体充分溶解在1 L水中得到0.1 mol·L-1的食盐水
C.将0.1 mol氧化钠溶于水并配成1 L溶液得到0.1 mol·L-1的NaOH溶液
D.同温时,溶解度越大的物质配得的饱和溶液的物质的量浓度不一定越大
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
400mL某溶液 中含有0.1mol Fe2+、0.2mol Fe3+加入0.2mol铁粉,待Fe3+反应完全后,溶液中Fe2+的物质的量浓度为(假设反应前后溶液体积不变)( )
中含有0.1mol Fe2+、0.2mol Fe3+加入0.2mol铁粉,待Fe3+反应完全后,溶液中Fe2+的物质的量浓度为(假设反应前后溶液体积不变)( )
A.0.4mol·L-1 B.0.6mol·L-1 C.0.8mol·L-1 D.1.0mol·L-1
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe-2e- Fe2+
Fe2+
C.电池充电过程中,阴极附近溶液的pH升高
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e- Ni2O3+3H2O
Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
下列物质①氢氟酸②浓硫酸③烧碱溶液④Na2CO3固体⑤硝酸⑥石灰石,其中在一定条件下能与SiO2反应的有( )
A.①② B.全部 C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三上第一次诊断化学试卷(解析版) 题型:填空题
氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
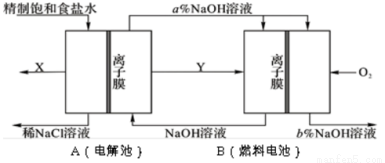
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期10月质检化学试卷(解析版) 题型:选择题
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )

A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.15 mol
D.K2Cr2O7与FeSO4反应的物质的量之比为1∶6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com