
【题目】请回答:
(1)用氧化物表示翡翠:NaAl(SiO3)2的组成___________________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________________。
(3)在NaHSO4溶液中滴加Ba(OH)2溶液恰好完全沉淀,写出反应的离子方程式____________
(4)写出化学反应方程式
①煅烧黄铁矿__________________________。
②用氨气制硝酸的第一步__________________________。
【答案】Na2O·Al2O3·6SiO2 2Mg+CO2![]() 2MgO+C SO42-+H++Ba2++OH-=BaSO4↓+H2O 4FeS2+11O2
2MgO+C SO42-+H++Ba2++OH-=BaSO4↓+H2O 4FeS2+11O2![]() 2Fe2O3+8SO2 4NH3+5O2
2Fe2O3+8SO2 4NH3+5O2![]() 4NO +6H2O
4NO +6H2O
【解析】
(1)根据化学式可知其氧化物形式可表示为Na2O·Al2O3·6SiO2;
(2)镁在二氧化碳中燃烧生成氧化镁和碳,反应的化学方程式为2Mg+CO2![]() 2MgO+C;
2MgO+C;
(3)NaHSO4溶液中滴加Ba(OH)2溶液恰好完全沉淀时生成硫酸钡、氢氧化钠和水,离子方程式为SO42-+H++Ba2++OH-=BaSO4↓+H2O;
(4)①煅烧黄铁矿的化学方程式为4FeS2+11O2![]() 2Fe2O3+ 8SO2;
2Fe2O3+ 8SO2;
②氨气催化氧化的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
【点晴】
硅酸盐用氧化物形式表示需要注意:氧化物的顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水。其次氧化物前系数配置原则:除氧元素外,其他元素按配置前后原子个数守恒原则配置系数。该题的另一个易错点是(3),答题时注意量的问题,如果硫酸氢钠过量,则生成硫酸钡、硫酸钠和水,解答时注意灵活应用。


科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种二元弱酸。室温时,下列指定溶液中微粒物质的量浓度关系正确的是
A.0.1 mol·L1 NaHC2O4溶液:c(Na+)>c(C2O![]() )>c(HC2O
)>c(HC2O![]() )
)
B.0.1 mol·L-1 Na2C2O4溶液:c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O![]() )
)
C.0.1 mol·L1 H2C2O4溶液:0.2 mol·L1 + c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O![]() )
)
D.向Na2C2O4溶液中滴加H2C2O4溶液至中性:c(Na+) = 2c(C2O![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的催化氧化反应:2SO2(g)+O2(g)![]() 2SO3(g)是工业制硫酸重要反应。
2SO3(g)是工业制硫酸重要反应。
(1)从平衡角度分析采用过量O2的原因是_____。
(2)某温度下,SO2的平衡转化率(![]() )与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)____K(B)(填“>”、“<”或“=”,下同)。
)与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)____K(B)(填“>”、“<”或“=”,下同)。
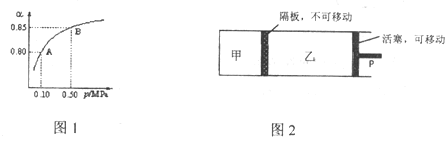
(3)保持温度不变,将等物质的量的SO2和O2混合气平分两份,分别加入起始体积相同的甲、乙两容器中,保持甲容器恒容,乙容器恒压到达平衡(如图2)。两容器的SO2的转化率关系为![]() 甲_____
甲_____![]() 乙。
乙。
(4)工业制硫酸的尾气中有少量SO2气体,可用NaClO2碱性溶液吸收,该反应的离子方程式为:___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应N2+3H2![]() 2NH3,用v(H2)和v(N2)分别表示其中的化合反应的速率,用v(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( )
2NH3,用v(H2)和v(N2)分别表示其中的化合反应的速率,用v(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( )
A.3v(N2)=v(H2)
B.v(H2)=v(NH3)
C.2v(H2)=3v(NH3)
D.v(N2)=3v(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A. 单位时间内生成n molA2同时生成n molAB
B. 容器内的总物质的量不随时间变化
C. 单位时间内生成2n molAB的同时生成n molB2
D. 单位时间内生成n molA2的同时生成n molB2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目。
(1)方案Ⅰ:有人提出将大小相等的铁片和铜片同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为_________________________。
(2)方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式______________________________________。
(3)方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):_________________________________________________;用离子方程式表示其反应原理:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:下表为25℃时某些弱酸的电离平衡常数。
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7Ka2=4.7×10﹣11 |
如图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )

A.Ⅰ曲线代表HClO,Ⅱ曲线代表CH3COOH
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO﹣+CO2+H2O=HClO+CO32-
C.图象中a、c两点处的溶液中![]() 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D.图象中a点酸的总浓度大于b点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:
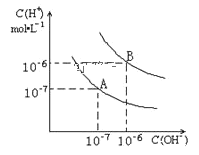
(1)25℃时,水的电离平衡曲线应为_________请说明理由_________
(2)95℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为_________
(3)95℃时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
(1)已知:H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) ΔH1=61kJ·mol-1
SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) ΔH2=-151kJ·mol-1
2HI(aq)=H2(g)+I2(g) ΔH3=110kJ·mol-1
则硫化氢气体分解为氢气和固体硫的热化学方程式为___。
(2)K2CO3溶液吸收H2S的反应为K2CO3+H2S![]() KHS+KHCO3,该反应的平衡常数的对数值为lgK=___
KHS+KHCO3,该反应的平衡常数的对数值为lgK=___
(已知:H2CO3lgK1=-6.4,lgK2=-10.3;H2SlgKl=-7.0,lgK2=-19.0)。
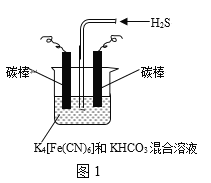
(3)工业上采用图1所示装置电解K4[Fe(CN)6]和KHCO3混合溶液一段时间,然后停止电解,通入H2S,利用生成的K3[Fe(CN)6]将H2S转化为S,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为___。
②通入H2S过程中,伴有CO![]() 转化为HCO
转化为HCO![]() 。通H2S发生反应的离子反应方程式为___。
。通H2S发生反应的离子反应方程式为___。
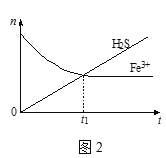
(4)将含H2S尾气的空气按一定流速通入酸性FeCl3溶液中,可实现含H2S尾气的空气脱硫。在FeCl3溶液吸收H2S的过程中,溶液中的n(Fe3+)及被吸收的n(H2S)随时间t的变化如图2所示。t1时刻后,溶液中n(Fe3+)保持微量减少至基本不变,其原因是___。
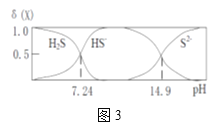
(5)H2S溶液中H2S、HS-,S2-的物质的量分数δ(X)随pH的变化如图3所示,H2S的电离平衡常数Ka1=___。写出pH由12.0变为16.0时发生的主要的离子方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com