
【题目】在常温下,把一个盛有一定量的甲烷和氯气的密闭玻璃容器放在光亮的地方,两种气体发生反应,下列叙述中不正确的是
A. 容器内原子的总数不变B. 容器内的分子总数不变
C. 容器内压强不变D. 发生的反应属于取代反应
科目:高中化学 来源: 题型:
【题目】下图表示某化学反应过程中,生成物的量与时间的关系,图中a、b、c三条曲线不能反映下列哪种因素对生成物的量的影响( )

A. 不同的温度 B. 不同的pH值
C. 不同的底物浓度 D. 不同的酶浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第周期,第族;
(2)X可形成双原子分子,其分子的电子式是;Y和氢元素形成的10电子微粒中常见的+1价阳离子为(填化学式,下同);Z和氢元素形成的18电子微粒中常见的﹣1价阴离子为;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2 , 该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡进有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
A. 22.4LO2中含有NA个氧分子
B. 将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L
C. 标准状况下,22.4LH2O中含有的水分子数是NA个
D. 3.4gNH3含有的氨分子数为0.2NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,①5gH2 ②11.2LO2 ③2molH2O ④6.02×1023个 CO2分子。
(1)5gH2 的物质的量是__________,体积是__________;
(2)6.02×1023个 CO2分子的物质的量是__________,质量是__________,
(3)所含分子数最多的是_________(请用序号回答,后同);
(4)所含原子数最多的是_________;
(5)质量最大的是_________;
(6)体积最大的是_________;
(7)气体密度最大的是_________;
(8)体积最小的是_________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO45H2O)及副产物ZnO.制备流程图如下: 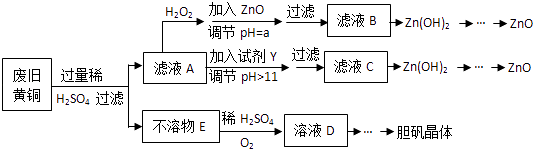
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2﹣下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算).
Fe3+ | Fe2+ | Zn2+ | |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)加入ZnO调节pH=a的目的是 , a的范围是 .
(2)由不溶物E生成溶液D的化学方程式为 .
(3)滤液A中加入H2O2反应的离子方程式为 .
(4)由溶液D制胆矾晶体包含的主要操作步骤是 .
(5)下列试剂可作为Y试剂的是 . A.ZnO B.NaOH C.Na2CO3D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中错误的是( )
A. 构成原电池的正极和负极必须是两种不同的金属
B. 原电池是将化学能转变为电能的装置
C. 在原电池中,电子流出的一极是负极,发生氧化反应
D. 原电池放电时,电流的方向是从正极到负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铝合金投入100mL一定物质的量浓度盐酸中,合金全部溶解,向所得溶液中滴加4mol /LNaOH溶液至过量,生成沉淀的质量与加入NaOH溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g),求:
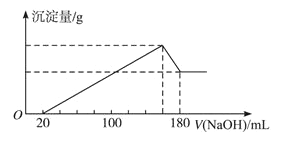
(1)原合金中Mg、Al质量各多少克?_________
(2)盐酸的物质的量浓度c(HCl)=____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol燃料完全燃烧的数据分别为:
燃料 | 一氧化碳 | 甲烷 | 异辛烷(C8H18) | 乙醇 |
△H | ﹣283.0kJmol﹣1 | ﹣891.0kJmol﹣1 | ﹣5461.0kJmol﹣1 | ﹣1366.8kJmol﹣1 |
使用上述燃料.最能体现“低碳经济”理念的是( )
A.一氧化碳
B.甲烷
C.异辛烷
D.乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com