
分析 (1)①平衡常数等于生成物的浓度系数次幂之积除以反应物浓度系数次幂之积;
②根据温度对平衡移动的影响判断反应热的符号;
③甲槽为CO2得电子发生还原反应生成CH3OH,据此书写反应式;
(2)根据平衡状态的本质和表观现象分析;
(3)①根据盖斯定律:1:CH4 (g)+H2O (g)=CO (g)+3H2 (g)△H=+206.0kJ•mol-1
2:CO (g)+2H2 (g)=CH3OH (g)△H=-129.0kJ•mol-1
依据盖斯定律,1+2得到要书写的热化学方程式.
②CH4(g)+H2O(g)$?_{催化剂}^{高温}$CO2(g)+3H2(g)
起始(mol/L):1 1 0 0
变化(mol/L):0.8 0.8 0.8 2.4
平衡(mol/L):0.2 0.2 0.8 2.4
此时CH4的转化率为$\frac{0.8}{1}$×100%=80%;
由图3可知,在7min时,氢气的浓度增大了一倍,可能是缩小体积为原来的$\frac{1}{2}$或增加了等量的氢气,平衡均是逆向移动.
解答 解:(1)①二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),其平衡常数K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}(H)}$,
故答案为:$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}(H)}$;
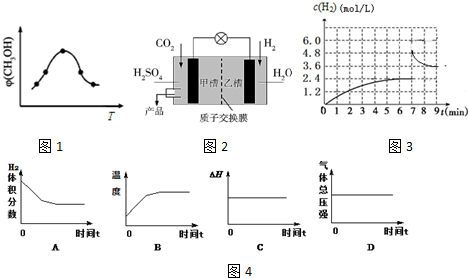
②根据图象可知达到平衡后,温度越高,甲醇的体积分数φ(CH3OH)越小,说明升高温度平衡逆移,则正反应方向为放热反应,则△H<0,
故答案为:<;
③根据图2,甲槽为CO2得电子发生还原反应生成CH3OH,反应式为CO2+6e-+6H+═CH3OH+H2O,
故答案为:CO2+6e-+6H+═CH3OH+H2O;
(2)A.在一定的时间后,氢气含量不变为平衡状态,故A正确;
B..在一定的时间后,温度不变为平衡状态,故B正确;
C.反应的焓变与反应是否达平衡无关,故C错误;
D.反应条件为恒压,故压强不变不能判断反应是否达平衡,故D错误.
故答案为:AB;
(3)①根据盖斯定律:1:CH4 (g)+H2O (g)=CO (g)+3H2 (g)△H=+206.0kJ•mol-1
2:CO (g)+2H2 (g)=CH3OH (g)△H=-129.0kJ•mol-1
依据盖斯定律,1+2得到:CH4(g)+H2O(g)=CH3OH (g)+H2(g))△H=+77kJ•mol-1,
故答案为:CH4(g)+H2O(g)=CH3OH (g)+H2(g))△H=+77kJ•mol-1;
②CH4(g)+H2O(g)$?_{催化剂}^{高温}$CO2(g)+3H2(g)
起始(mol/L):1 1 0 0
变化(mol/L):0.8 0.8 0.8 2.4
平衡(mol/L):0.2 0.2 0.8 2.4
此时CH4的转化率为$\frac{0.8}{1}$×100%=80%;
由图3可知,在7min时,氢气的浓度增大了一倍,可能是缩小体积为原来的$\frac{1}{2}$或增加了等量的氢气,无论是增大压强,还是增大氢气的浓度,平衡均是逆向移动,
故答案为:80%;逆反应;将容器体积缩小为原来的$\frac{1}{2}$或加入等量的氢气.
点评 本题考查了盖斯定律的应用、化学平衡影响因素和化学平衡常数以及转化率的计算、燃料电池的电极反应式的书写,综合性较强,为历年高考高频考点,侧重于化学反应原理和图象分析能力的培养,题目难度中等.


科目:高中化学 来源: 题型:解答题
 .
.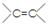 两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.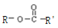 +H2O
+H2O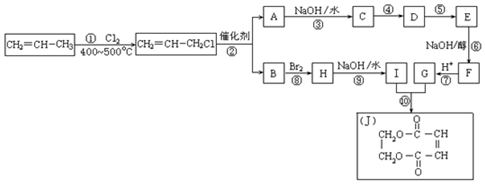
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,22.4LCCl4中含5 NA个原子 | |
| B. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1 NA | |
| C. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1 NA | |
| D. | 将100mL0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液中先滴足量盐酸无现象,再滴加BaCl2溶液有白色沉淀,说明原溶液中有SO42- | |
| C. | 某溶液中滴加NaOH溶液有蓝色沉淀,说明原溶液中有Fe3+ | |
| D. | 某溶液中滴加稀硫酸生成无色气体,说明原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
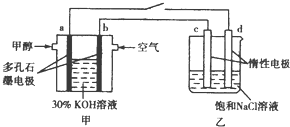 CO2是一种温室气体,据科学家预测,到21世纪中叶,全球气温将升高1.5-4.5℃,地球气温的升高会引起海平面升高,对人类的生存环境产生巨大的影响.如何合理地利用CO2是摆在科学家面前的一个重大课题.回答下列问题:
CO2是一种温室气体,据科学家预测,到21世纪中叶,全球气温将升高1.5-4.5℃,地球气温的升高会引起海平面升高,对人类的生存环境产生巨大的影响.如何合理地利用CO2是摆在科学家面前的一个重大课题.回答下列问题:| CO2的量 | NaOH溶液的量 | 放出的热量 | |
| ① | 22.0g | 750mL1.0mol•L-1 | xkJ |
| ② | 1.0mol | 2.0mL1.0mol•L-1 | ykJ |
| 物质 | CO2(g) | H2(g) | CH4(g) | H2O(g) |
| 浓度/mol•L-1 | 0.2 | 0.8 | a | 1.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
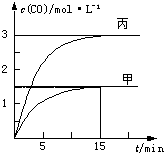 一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )
一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )| 容 器 | 甲 | 乙 | 丙 |
| 容 积 | 0.5L | 0.5L | V |
| 温 度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2molC 1molH2O | 1molCO 1molH2 | 4molC 2molH2O |
| A. | 甲容器中,反应在前15min的平均速率v(H2)=0.2mol•L-1•min-1 | |
| B. | 丙容器的体积V>0.5L | |
| C. | 当温度为T1℃时,反应的平衡常数K=4.5(mol•L-1) | |
| D. | 乙容器中,若平衡时n(H2O)=0.4mol,则T1<T2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器Ⅰ、Ⅱ中正反应速率相同 | |
| B. | 容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深 | |
| C. | 容器Ⅰ、Ⅲ中反应的平衡常数相同 | |
| D. | 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑤ | C. | ③④⑤⑥ | D. | ④⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com