
����Ŀ�����÷Ͼ������Ͻ���Ҫ�ɷ�ΪFe��Al��Fe2O3��Al2O3���Ʊ����ײ��ϴ���Fe3O4���Ӽ�������Al���Ʊ�����ͼ��ͼ�� 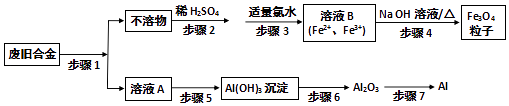
�ش��������⣺
��1������1�����õ��Լ��� �� �漰�Ļ�ѧ��Ӧ������������ԭ��Ӧ�Ļ�ѧ����ʽΪ
��2������3�з�Ӧ�����ӷ���ʽΪ ��
��3������5��ѡ�õ��Լ���������������������ţ��� a��NaOH��Һ b����ˮ c������ d��ͨ�������CO2
��4������7��ÿ��ø�����Al 27g��ת�Ƶĵ�����ĿΪ ��
��5�����й��ڴ���Fe3O4���ӵ�˵����ȷ����������ţ���
A.����Fe3O4���ӻ���������ЧӦ
B.����Fe3O4���ӵĻ�ѧ������ԭ����Fe3O4��ȫ��ͬ
C.����Fe3O4�������ڽ����ɢϵ
D.����Fe3O4����������ֽ��
���𰸡�
��1��NaOH��Һ��2Al+2NaOH+2H2O=2NaAlO2+3H2��
��2��2Fe2++Cl2=2Fe3++2Cl��
��3��d
��4��3NA��1.806��1024
��5��D
���������⣺��1��������֪����1�Ǽ�������������Һ�ܽ�Al��Al2O3 �� ����������ԭ��Ӧ������������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2�������Դ��ǣ�NaOH��Һ��2Al+2NaOH+2H2O=2NaAlO2+3H2������2������3�з�Ӧ�����ӷ���ʽΪ�������������������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2 Fe3++2Cl�� ��
���Դ��ǣ�2Fe2++Cl2=2 Fe3++2Cl������3������5��ѡ�õ��Լ����γ���������������
a��NaOH��Һ��ƫ�����ƣ���a����
b����ˮ��ƫ�����Ʋ���Ӧ������������������������b����
c�������ƫ��������Һ��Ӧ�������ɵ����������������ڹ��������ᣬ������ã���c����
d��ͨ�������CO2 ��ƫ��������Һ��Ӧ��������������������ȫ�����������ӣ���d��ȷ��
���Դ��ǣ�d����4������7�ǵ����������������Ӧ�Ļ�ѧ����ʽΪ��2Al2O3 ![]() 4Al+3O2��������4molAl������ת��12mol������Al 27g���ʵ���=
4Al+3O2��������4molAl������ת��12mol������Al 27g���ʵ���= ![]() =1mol������ת��3mol��Ϊ3NA��1.806��1024 ��
=1mol������ת��3mol��Ϊ3NA��1.806��1024 ��
���Դ��ǣ�3NA ��1.806��1024����5��A������Fe3O4���Ӳ��ǽ��壬��A����
B������Fe3O4���ӵĻ�ѧ������ԭ����Fe3O4��ͬ����B����
C������Fe3O4����Ϊ�����������ڽ����ɢϵ����C����
D������Fe3O4������������������ֽ����D��ȷ��
���Դ��ǣ�D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��ķ�Ӧԭ�������ӷ���ʽ��ʾ��ȷ���ǣ� ��
A.������ˮ��Al3++3H2O=Al��OH��3��+3H+
B.�ù�����ˮ���չ�ҵβ���е�SO2��2NH3?H2O+SO2=2NH4++SO32��+H2O
C.��CuCl2��Һ������ʵ�飬���ݷ��⣺CuCl2 ![]() Cu2++2C1��
Cu2++2C1��
D.�ø�����ر���Һ�ζ����2MnO4��+16H++5C2O42��=2Mn2++10CO2��+8H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����������ĵ���ƽ�ⳣ�����£�
���� | CH3COOH | H2CO3 | H2SO3 |
����ƽ�ⳣ�� | K=1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=1.5��10-2 K2=1.02��10-7 |
��1��CH3COOH��H2CO3��H2SO3��������������������__________(�ѧʽ)��
��2��CH3COOH�ĵ���ƽ�ⳣ������ʽΪK=__________��
��3��д��H2CO3�ĵڶ������뷽��ʽ��_____________��
��4��д��H2SO3��Һ��CH3COONa��Һ��Ӧ�����ӷ���ʽ��____________________��
��5���������Ϊ10mL��pH��Ϊ2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1000mL��ϡ������pH�ı仯��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��____________(������������ С��������������)����ĵ���ƽ�ⳣ����������__________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ַdz���Ҫ�Ļ���ԭ�ϣ��ڹ�ҵ�Ϻ�ʵ���������Ź㷺��Ӧ�ã�
��1�������⣨��Ҫ�ɷ�ΪFe2O3����д����Ӧԭ�������ӷ���ʽ��
��2���Ʊ��轺����ҵ�Ͽ�����ˮ���������ᷴӦ�Ʊ������һ�������ɵõ��轺��д��ˮ���������ᷴӦ�Ļ�ѧ����ʽ��
��3����������ʵ���ҿ�������Ũ���������س����·�Ӧ����ȡ������ ��Ӧͬʱ��������MnCl2��KCl��H2O��д���÷�Ӧ�Ļ�ѧ����ʽ �� �ڴ˷�Ӧ��������ֳ����ԣ�
��4����ҵ�Ͽ���������ͼ��ʾװ���Ʊ����ᣬ����������A��B������ͨ����������ȼ��Ȼ����������A��B������ͨ���������з�Ӧ����ʱ�������ɫΪ �� ���������������� �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��һ���¶����У�a�����ᡡb�����ᡡc��������������Һ���������abc��գ�
���������ʵ���Ũ����ͬʱ��c��H+���ɴ�С��˳����__________��
������pH��ͬʱ�����ʵ���Ũ���ɴ�С��˳��Ϊ_________������ϡ��10����pH�ɴ�С��˳��Ϊ_____________
��2��ij�¶��£���ˮ�е�c (H+)= 4.0��10-7 mol/L, ����¶��´�ˮ�е�c (OH-)=______________mol/L; ���¶Ȳ���, ����ϡNaOH��Һ, ʹc (OH-)= 5.0��10-6 mol/L,����Һ��c (H+)= _________________mol/L.
��3����25��ʱ��100ml 1.0mol/L������������1.2mol/L������������Һ���, ��Ϻ���Һ��pH= _______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ���ǣ� ��
A.1L pH=l��������Һ�к��е�H+��ĿΪ0.2NA
B.1 mol�ǻ���l mol����������������������Ϊ9NA
C.14 g��N2��CO��ɵĻ�������к��е�ԭ����ĿΪ2NA
D.��״���£�2.24 L Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������立ֽⷴӦ�У����ɵĺ��������н��е������������֣����б������ĵ�Ԫ�غͱ���ԭ�ĵ�Ԫ�����ʵ���֮��Ϊ( )
A. 5��3 B. 1��1 C. 5��4 D. 3��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ�����
�����ж���ȷ����
A. ����c(CO)��ƽ���������ƶ�����Ӧ��ƽ�ⳣ������
B. ��һ�Σ���30����50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
C. �ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
D. �÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����ԼΪ22.4L���ǣ� ��
A.��״����1molH2O
B.20�桢101kPaʱ36.5gHCl
C.���³�ѹ��17gNH3
D.��״����0.4mol H2��0.6molO2�Ļ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com