

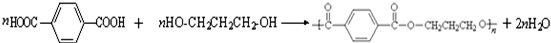 ��
�� ��������Ƴ������ķ�Ӧ����ͼ��
��������Ƴ������ķ�Ӧ����ͼ��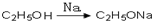 ��
��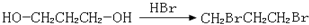 ��
�� ��
�� ���� ��1��A�����������ӳɷ�Ӧ����1��3-��������A�к��в����ͼ�������������CO�����������ӳɷ�Ӧ����A��A�к���-CHO����ϩȩת��ΪA��Ӧ����ˮ�����ӳɷ�Ӧ����AΪHOCH2CH2CHO��
��2������ԭ�ϵ��Ƿ�Ϊ��������Դ�����жϣ�
��3��1��3-��������Ա�������ɷ������۷�Ӧ���Դ˿���д��Ӧ�Ļ�ѧ����ʽ��
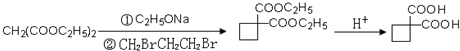
��4���������⣬Ӧ������C2H5ONa��CH2BrCH2CH2Br��Ȼ����������������Ӧ������Ŀ���
��� �⣺��1��A�����������ӳɷ�Ӧ����1��3-��������A�к��в����ͼ�������������CO�����������ӳɷ�Ӧ����A��A�к���-CHO����ϩȩת��ΪA��Ӧ����ˮ�����ӳɷ�Ӧ����AΪHOCH2CH2CHO��
�ʴ�Ϊ��CH2OHCH2CHO��
��2����ɫ��ѧ�ǵ��³�������Ҫ���ǿɳ�������Դ�������⣬·��3�Կ�������Դ����Ϊԭ�ϣ�·��1��2��ԭ��Ϊʯ�Ͳ�Ʒ����ʯ���Dz���������Դ��
�ʴ�Ϊ��3��·��3�Կ�������Դ����Ϊԭ�ϣ�·��1��2��ԭ��Ϊʯ�Ͳ�Ʒ����ʯ���Dz���������Դ��
��3��1��3-��������Ա�������ɷ������۷�Ӧ����Ӧ�ķ���ʽΪ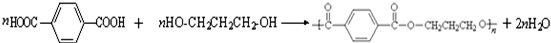 ��
��
�ʴ�Ϊ��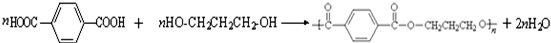 ��
��
��4���������⣬Ӧ������C2H5ONa��CH2BrCH2CH2Br��Ȼ����������������Ӧ������Ŀ���������Ӧ�Ĺ���Ϊ����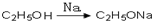 ����
����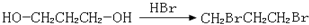 ����
���� ��
��
�ʴ�Ϊ��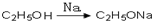 ��
��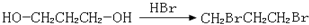 ��
�� ��
��
���� ���⿼���л���ĺϳɣ���Ŀ�Ѷ��еȣ���4��Ϊ�״��㣬������Ŀ�������Ϣ�ǹؼ��������Ŀ��ʱ��ע����չ����ŵĽṹ�����ʣ����ݹ����ŵı仯���з�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ƬͶ���ռ���ҺAl+2OH-�TAlO2-+H2�� | |
| B�� | ������ˮ��ӦCl2+H2O?2H++Cl-+ClO- | |
| C�� | ̼�����������CO32-+2H+�TH2O+CO2�� | |
| D�� | �����Ƹ�ˮ��Ӧ2Na+2H2O�T2Na++2OH-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢� | C�� | �ڢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���淴ӦaA��g��+bB��g��?cC��g��+dD��g������Hͬʱ����������ͼ�и����ߵĹ��ɵ��ǣ�������
���淴ӦaA��g��+bB��g��?cC��g��+dD��g������Hͬʱ����������ͼ�и����ߵĹ��ɵ��ǣ�������| A�� | a+b��c+d T1��T2��H��0 | B�� | a+b��c+d T1��T2��H��0 | ||
| C�� | a+b��c+d T1��T2��H��0 | D�� | a+b��c+d T1��T2��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ڳ����£�ijˮ��ҺM�У�
�ڳ����£�ijˮ��ҺM�У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
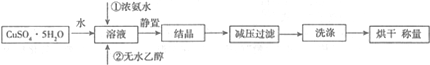

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
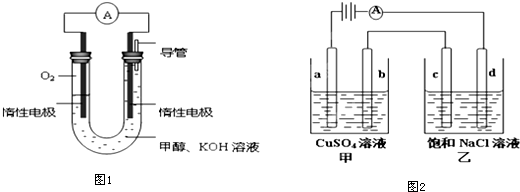
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com