
(12分)
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究。下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)
①该研究小组在设计方案时。考虑了浓度、 、 等因素对过氧化氢分解
速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率有何影响?
。
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
①该反应的化学方程式为 ;
②从开始至2min,Z的平均反应速率为 ;2min后Z的生成速率与2min末Z的生成速率 (“是”或“否”)相等,理由是 。
① 温度、催化剂
②其他条件不变时,升高温度化学反应速率增大或加催化剂化学反应速率增大等等
(2)① 3X + Y2Z; ② 0.05mol/(L·min); 是,2min时,反应达到了平衡,各物质的物质的量浓度不再改变,反应速率也不再改变。
解析:(1)考查外界条件对反应速率的影响。根据反应条件可判断,在实验中主要考虑的是浓度、温度、催化剂对反应速率的影响。根据实验现象可知其他条件不变时,升高温度化学反应速率增大,使用催化剂化学反应速率增大。
(2)根据图像可判断,X、Y是反应物,Z是生成物。反应进行到2min时,X、Y、Z的变化量(mol)分别是0.3、0.1、0.2,根据变化量之比是相应的化学计量数之比可知反应的方程式为
3X + Y2Z。反应速率通常用单位时间内浓度的变化量来表示,所以从开始至2min,Z的平均反应速率为
![]() 。由图像可判断,反应进行到2min时,各种物质的物质的量均不再随时间变化而变化,所以反应达到化学平衡状态,因此2min后Z的生成速率与2min末Z的生成速率是相等的。
。由图像可判断,反应进行到2min时,各种物质的物质的量均不再随时间变化而变化,所以反应达到化学平衡状态,因此2min后Z的生成速率与2min末Z的生成速率是相等的。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,使木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
| ||
| ||
| 双氧水体积 | 操作情况 | 反应完成所需的时间 | 收集到气体体积 | 反应后液体温度 |
| a1%的150mL | 11分钟 | 539mL | 24℃ | |
| a2%的15mL | 混合不振荡 | 1分20秒 | 553mL | 56℃ |
| a3%的7.5mL | 9秒 | 562mL | 67℃ |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖南省望城一中高一下学期期中考试化学试卷(带解析) 题型:填空题
(12分)
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究。下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)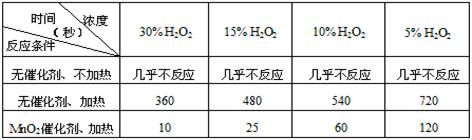
①该研究小组在设计方案时。考虑了浓度、 、 等因素对过氧化氢分解
速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率有何影响?
。
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白: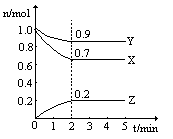
①该反应的化学方程式为 ;
②从开始至2min,Z的平均反应速率为 ;2min后Z的生成速率与2min末Z的生成速率 (“是”或“否”)相等,理由是 。
查看答案和解析>>
科目:高中化学 来源:2014届湖南省高一下学期期中考试化学试卷(解析版) 题型:填空题
(12分)
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究。下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)
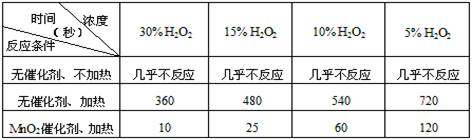
①该研究小组在设计方案时。考虑了浓度、 、 等因素对过氧化氢分解
速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率有何影响?
。
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
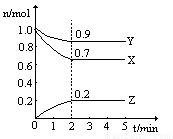
①该反应的化学方程式为 ;
②从开始至2min,Z的平均反应速率为 ;2min后Z的生成速率与2min末Z的生成速率 (“是”或“否”)相等,理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com