
【题目】某有机物F(![]() )是有机合成的中间体。现以甲苯为原料合成F的路线如图所示。
)是有机合成的中间体。现以甲苯为原料合成F的路线如图所示。

已知:①R-CN![]() R-COOH
R-COOH
②
回答下列问题:
(1)A→B的反应试剂是___。
(2)B→C反应的化学方程式为___,反应类型是___。D→E的反应类型是___。
(3)D中含氧官能团的名称是___。
(4)G是F的同系物,比F多一个碳原子,其苯环上含两个取代基的同分异构体有___种(不考虑立体异构)。其中核磁共振氢谱有六组峰,且峰面积之比为1:1:1:2:2:3的有机物结构简式为___。
(5)结合以上合成路线及相关信息,设计由苯合成苯酚的合成路线___。(用合成流程图表示,并注明反应条件)
【答案】浓硫酸、浓硝酸 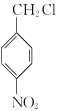 +NaCN
+NaCN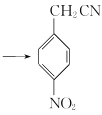 +NaCl 取代反应 还原反应 羧基、硝基 6
+NaCl 取代反应 还原反应 羧基、硝基 6 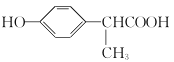
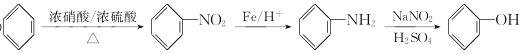
【解析】
甲苯与Cl2光照下发生侧链上的取代反应生成A,A的结构简式为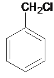 ,分子式为C7H7Cl,对比B和A的分子式,少了1个H原子,多了NO2,则可知A到B为硝化反应,结合F的结构简式,可知B的结构简式为
,分子式为C7H7Cl,对比B和A的分子式,少了1个H原子,多了NO2,则可知A到B为硝化反应,结合F的结构简式,可知B的结构简式为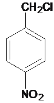 。对比C和B的分子式,B转化为C过程是B中的氯原子被-CN取代,C的结构简式为
。对比C和B的分子式,B转化为C过程是B中的氯原子被-CN取代,C的结构简式为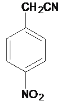 。根据已知,C转化为D,-CN变成了-COOH,D的结构简式为
。根据已知,C转化为D,-CN变成了-COOH,D的结构简式为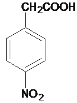 。根据已知,D转化为E发生题给已知②的反应,D中-NO2被还原为-NH2,E的结构简式为
。根据已知,D转化为E发生题给已知②的反应,D中-NO2被还原为-NH2,E的结构简式为 ;结合E和F的结构简式,可知E中-NH2转化为-OH,生成F。
;结合E和F的结构简式,可知E中-NH2转化为-OH,生成F。
(1) A的结构简式为 ,分子式为C7H7Cl,对比B和A的分子式,少了1个H原子,多了NO2,则可知A到B为硝化反应,硝化反应的反应试剂是浓硝酸、浓硫酸;
,分子式为C7H7Cl,对比B和A的分子式,少了1个H原子,多了NO2,则可知A到B为硝化反应,硝化反应的反应试剂是浓硝酸、浓硫酸;
(2) 对比C和B的分子式,B转化为C过程是B中的氯原子被-CN取代,化学方程式为 +NaCN→
+NaCN→ +NaCl,为取代反应。根据已知,D转化为E发生题给已知②的反应,D中-NO2转化为-NH2,整个过程“加氢去氧”,为还原反应;
+NaCl,为取代反应。根据已知,D转化为E发生题给已知②的反应,D中-NO2转化为-NH2,整个过程“加氢去氧”,为还原反应;
(3) D的结构简式为 ,其含氧官能团的名称为羧基、硝基;
,其含氧官能团的名称为羧基、硝基;
(4) G是F的同系物,则G也有1个-COOH,1个-OH,其中-OH直接与苯环相连;比F多一个碳原子,苯环上含两个取代基,则其中一个取代基为—OH,另一个取代基上有3个C原子,包括了1个-COOH,则取代的结构有—CH2CH2COOH、-CH(CH3)COOH,共2种。在苯环上,2个取代基,有邻、间、对,三种位置,则同分异构体共2×3=6种。其中核磁共振氢谱有六组峰,且峰面积之比为1:1:1:2:2:3;其中的3说明,有1个-CH3;其中的2:2,说明2个取代基处为对位,则结构简式为 ;
;
(5)由苯合成苯酚,物质F中含有酚羟基,其来源于-NO2,因此可以模范路线中-NO2转化为-OH的过程,过程为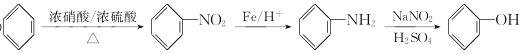 。
。


科目:高中化学 来源: 题型:
【题目】硼铁混合精矿含有硼镁石[MgBO2(OH)、磁铁矿(Fe3O4)、磁黄铁矿(FexS)、品质铀矿(UO2)等,以该矿为原料制备MgSO4·H2O和硼酸(H3BO3)的工艺流程如下:
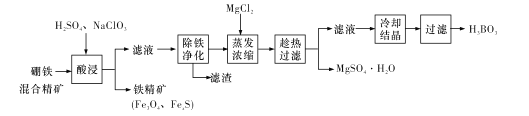
已知:![]() 在pH为4~5的溶液中生成UO2(OH)2沉淀。
在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
(l)“酸浸”时,为了提高浸出率可采取的措施有:________ (至少答两个措施),该步骤中NaC1O3可将UO2转化为![]() ,则该反应的离子方程式为_____。
,则该反应的离子方程式为_____。
(2)“除铁净化”需要加入____(填化学式)把溶液pH调节至4~5,滤渣的成分是_______。
(3)“蒸发浓缩”时,加入固体MgC12的作用是 ___。
(4)铁精矿(Fe3O4、FexS)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃,
![]() ,
,![]() ,
,![]() 回答下列问题:
回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:![]() ,则该条件下Fe3+水解反应的平衡常数K= __(用含以的字母表示)。
,则该条件下Fe3+水解反应的平衡常数K= __(用含以的字母表示)。
②在T℃向饱和Fe(OH)3、Fe(OH)2的混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的c(Fe2+)/c(Fe3+)会 __(填“变大”“变小”或“不变”),请结合相关数据推理说明:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原电池的知识,下列反应可设计成原电池的是( )
A.CH3CH2OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
B.Ba(OH)28H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
C.H2SO4+2NaOH=Na2SO4+2H2O
D.CaO+H2O=Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用相同浓度的NaOH溶液,分别滴定20mL0.1mol·L-1的三种酸(HA、HB和HD)溶液体积的变化曲线如图所示。下列判断正确的是( )
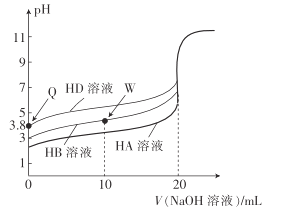
A.由Q点可知,HD的电离平衡常数Ka≈10-7.6
B.三种酸的酸性强弱:HD>HB>HA
C.滴定至W点时,溶液中存在:c(B-)>c(Na+)>c(H+)>c(OH-)
D.当三种溶液恰好完全中和后将其混合,溶液中存在:c(Na+)=c(A-)+c(B-)+c(D-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.100 mL 1 mol·L-1 NaClO溶液中ClO-的数目为0.1NA
B.46 g 75%的C2H5OH溶液中所含O原子数目为0.75NA
C.7.6 g过氧乙酸(CH3COOOH)所含过氧键数目为0.1NA
D.标准状况下,22.4 L 氯气与水充分反应转移电子数目NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发新型储氢材料是开发利用氢能的重要研究方向。
(1)![]() 是一种储氢材料,可由
是一种储氢材料,可由![]() 和
和![]() 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为 _______,该电子层具有的原子轨道数为 _______。
②Li、B、H元素的电负性由大到小的排列顺序为 ___________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+ ___________(填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
|
|
|
|
|
738 | 1451 | 7733 | 10540 | 13630 |
则M是 ______________ (填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喹啉(![]() )是治疗新冠肺炎的药物氯喹的基础原料,其合成路线如下:
)是治疗新冠肺炎的药物氯喹的基础原料,其合成路线如下:
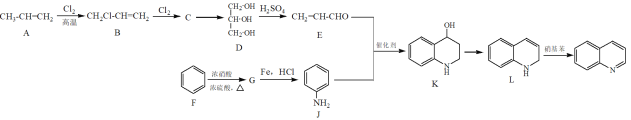
下列有关说法正确的是
A.C→D的反应条件为NaOH水溶液,加热
B.可以用溴水来检验化合物E中的碳碳双键
C.F→G和G→J的反应类型分别为取代反应和还原反应
D.与喹啉互为同分异构体,且含有碳碳双键和氰基(-CN)的芳香族化合物共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨、石墨烯及金刚石是碳的同素异形体。
(1)以Ni—Cr—Fe为催化剂,一定条件下可将石墨转化为金刚石。基态Fe原子未成对电子数为________。设石墨晶体中碳碳键的键长为am,金刚石晶体中碳碳键的键长为bm,则a________(填“>”“<”或“=”)b,原因是_______。
(2)比较表中碳卤化物的熔点,分析其熔点变化的原因是_________。
CCl4 | CBr4(α型) | CI4 | |
熔点/℃ | -22.92 | 48.4 | 168(分解) |
(3)金刚石的晶胞如图1所示。已知ZnS晶胞与金刚石晶胞排列方式相同,若图1中a与ZnS晶胞中Zn2+位置相同,则S2-在ZnS晶胞中的位置为________。

(4)石墨烯中部分碳原子被氧化后,转化为氧化石墨烯。
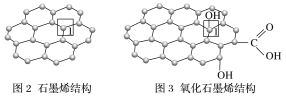
①在图3所示的氧化石墨烯中,采取sp3杂化形式的原子有________(填元素符号)。
②石墨烯转化为氧化石墨烯时,1号C与相邻C原子间键能的变化是________(填“变大”“变小”或“不变”)。
(5)石墨烯具有很大的比表面积,有望用于制超级电容器。若石墨烯中碳碳键的键长为am,12g单层石墨烯单面的理论面积约为________m2(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物结构为: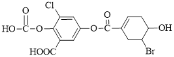 ,下列说法中正确的是
,下列说法中正确的是
A.该物质的化学式为C15H8O8BrCl
B.该物质能与FeCl3 溶液发生显色反应
C.1 mol 该物质最多能与 2 mol 溴水发生反应
D.一定条件下,1 mol 该物质最多能与 9 mol NaOH 反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com