
下列说法中不正确的是( )
①质子数相同的微粒一定属于同种元素
②同位素的性质几乎完全相同
③质子数相同、电子数也相同的微粒,不可能是一种分子和一种离子
④电子数相同的微粒不一定是同一种元素
⑤一种元素只能有一种质量数
⑥某种元素的相对原子质量取整数就是其质量数
A. ①②④⑤ B. ③④⑤⑥ C. ②③⑤⑥ D. ①②⑤⑥
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
对于可逆反应A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1 B.v(B)=1.2 mol·L-1·s-1
C.v(D)=0.4 mol·L-1·min-1 D.v(C)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2017届北京市朝阳区高三第一次(3月)综合练习理综化学试卷(解析版) 题型:填空题
我国每年产生的废旧铅蓄电池约330万吨。从含铅废料(PbSO4、PbO2、PbO等)中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下:

(1)铅蓄电池放电时,PbO2作____极。
(2)过程I,已知:PbSO4、PbCO3的溶解度(20℃)见图l;Na2SO4、Na2CO3的溶解度见图2。
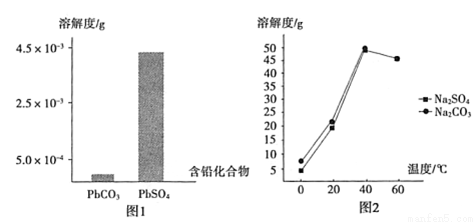
①根据图l写出过程I的离子方程式:__________。
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释可能原因:
i.温度降低,反应速率降低; ii.____(请你提出一种合理解释)。
③若生产过程中温度低于40℃,所得固体中,含有较多Na2SO4杂质,原因是____。
(3)过程Ⅱ,发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。实验中检测到有大量O2放出,推测PbO2氧化了H2O2,通过实验证实了这一推测。实验方案是____。
(已知:PbO2为棕黑色固体;PbO为橙黄色固体)
(4)过程Ⅲ,将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液,生成Pb,如图3。

①阴极的电极反应式是____________。
②电解一段时间后,PbCl2'浓度极大下降,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
下列实验不能作为判断依据的是( )
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱
C.硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
用铝热法还原下列化合物,制得金属的物质的量各 1 mol,需消耗铝最少的是
A.MnO2 B.Co3O4 C.WO 3 D.Cr2O3
3 D.Cr2O3
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:填空题
填空题
(1)H、D、T三种原子,它们之间的关系是_________;在标准状况下,它们的单质的密度之比为_____;1 mol各单质中,它们的质子数之比为________;在标准状况下,1L各种单质中,它们的电子数之比为________。
(2)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为垃,该元素在元素周期表中的位置是_____,属于______元素(填“金属”或“非金属”),若该元素存在最高价氧化物对应的水化物,则其化学式为_______。
(3)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(A~G)填入相应的空格中:

①IIA族元素的价电子数__________;②第三周期元素的最高正化合价____________;
③VIIA族元素氢化物的沸点____________。
(4)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为_____mol。
①若R为钙元素,且N=19,则采用原子符号的表达方式,可将R2+表示为_______;
②若R为第五周期IIA元素,则其硫酸盐______于水(填“溶”或“不溶”)。
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:选择题
己知短周期元素的四种离子:aA3+、bB+、。C2-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
A. 原子序数d>c>b>a B. 单质的还原性D<C<B<A
C. 离子半径C2->D->B+>A3+ D. 离子的氧化性A3+<B+
查看答案和解析>>
科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:填空题
新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是 ,B原子的杂化轨道类型是 .
Li、B、H元素的电负性由大到小排列顺序为 .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是 (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为 ,NaH的理论密度是 g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A. 元素W、X的氯化物中,各原子均满足8电子的稳定结构
B. 元素X与氢形成的原子比为1:1的化合物有很多种
C. 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D. 元素Z可与元素X形成共价化合物XZ2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com