
����Ŀ�������仯����㷺���������ǵ��ճ������ҵ�����С��ش��������⣺
(1)��̬Feԭ�ӵĺ�������Ų�ʽ��________��CaԪ����FeԪ��ͬ���ڣ�����![]() ������Ϊש��ɫ��������ȼ�ŵ�����䷽�г�����CaԪ�أ�����CaԪ�س���������ɫ��ԭ����____
������Ϊש��ɫ��������ȼ�ŵ�����䷽�г�����CaԪ�أ�����CaԪ�س���������ɫ��ԭ����____
(2)������Ѫ�쵰�Ľṹ��ʽ��ͼ��ʾ��
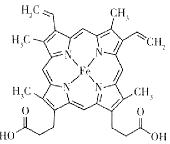
�����Ѫ�쵰��5��Ԫ���У��縺���ɴ�С��˳����_________��C��N��O�ĵ�һ�������ɴ�С��˳����_______��
��Ѫ�쵰���ӽṹ��N���ӻ���ʽ��_______��
��Ѫ�쵰���ӽṹ�к�����λ����Ϊ��Щ��λ���ṩ�µ��ӶԵ�Ԫ����_______(дԪ�ط��ţ���ͬ)���ṩ�չ����Ԫ����______��
(3)![]() ��Ӧ���ڹ�ҵ�����еĴ������侧���ṹ��ͼ��ʾ��
��Ӧ���ڹ�ҵ�����еĴ������侧���ṹ��ͼ��ʾ��
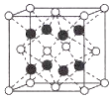
����֪�縺�ԣ�Fe-1.83��Br-2.96����![]() �к��еĻ�ѧ������Ϊ_________��
�к��еĻ�ѧ������Ϊ_________��
��![]() ���������������_________��
������������λ����_________��![]() �����߳�Ϊa cm����
�����߳�Ϊa cm����![]() �����ܶȵı���ʽΪ_____________
�����ܶȵı���ʽΪ_____________![]() (�谢���ӵ�������ֵΪNA)��
(�谢���ӵ�������ֵΪNA)��
���𰸡�![]() ����̬�ĵ���ԾǨ����̬ʱ�ͷų����� O>N>C>H>Fe N>O>C
����̬�ĵ���ԾǨ����̬ʱ�ͷų����� O>N>C>H>Fe N>O>C ![]() N Fe ���ۼ� 8
N Fe ���ۼ� 8 ![]()
��������
(1)Feԭ��Ϊ26��Ԫ�أ����������Ų�ʽΪ![]() (��
(��![]() )�����ӴӼ���̬ԾǨ����̬ʱ�ͷų��������Թ����ʽ�ͷš�
)�����ӴӼ���̬ԾǨ����̬ʱ�ͷų��������Թ����ʽ�ͷš�
(2)��һ������£�����Ԫ�صĵ縺�Աȷǽ���Ԫ�ص�����ͬ���ڴ����ң��縺������ǿ���ʵ縺�ԣ�O>N>C>H>Fe��N�ĺ�������Ų�ʽΪ![]() ������p�����3�����ӣ����ڰ����״̬�����ȶ�����N�ĵ�һ�����ܴ���O�����Ե縺�ԣ�N>O>C��
������p�����3�����ӣ����ڰ����״̬�����ȶ�����N�ĵ�һ�����ܴ���O�����Ե縺�ԣ�N>O>C��
��̼��˫���е�NΪ![]() �ӻ�������������Ϊ������NΪ
�ӻ�������������Ϊ������NΪ![]() �ӻ���
�ӻ���
����Ѫ�쵰�Ľṹ��ʽ��֪N��Fe�γ�2����λ����N�ṩ�¶Ե��ӣ�Fe�ṩ�չ����
(3)��Fe��Br�縺��֮��С��1.7����Ϊ���ۼ���
����![]() �����ṹ��֪����Fe�Ⱦ����������Br��8������
�����ṹ��֪����Fe�Ⱦ����������Br��8������![]() ������֪��1�������к�8��Br������4��Fe����1������������
������֪��1�������к�8��Br������4��Fe����1������������![]() �������V=a3 cm3�������ܶ�Ϊ
�������V=a3 cm3�������ܶ�Ϊ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��һ�ּ�������ˮ�Ҽ���������ˮ��Ӧ�Ļ���ɫ����(�е�11��)��ʵ�����Ʊ�����ClO2��Һ��װ����ͼ��ʾ��

��֪���з�Ӧ��NaClO3+HCl��NaCl+ClO2+Cl2+H2O��NaClO2+HCl��NaCl+ClO2+H2O��NaClO2+Cl2��NaCl+ClO2(��δ��ƽ)������˵����ȷ����
A.a��ͨ���N2����CO2��SO2����B.b��NaClO2���ñ���ʳ��ˮ����
C.c�й��ƿ��÷��ڱ�ˮԡ����ȴD.d������β����ֻ����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��һ�廷����(![]() )��NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽����
)��NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽����
�ף���Ӧ���Һ�е���ϡ�����к�NaOH��Ȼ���ٵ���AgNO3��Һ������dz��ɫ�����������֤����������ȥ��Ӧ��
�ң���Ӧ���Һ�е�����ˮ������Һ��ɫ�ܿ���ȥ�����֤����������ȥ��Ӧ��
������Ӧ���Һ�е�������KMnO4��Һ������Һ��ɫ��dz�����֤����������ȥ��Ӧ��
������ȷ���ǣ� ��
A. �� B. �� C. �� D. ����ʵ�鷽��������ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͬϵ�����ִ�������Ⱦ�����Ҫ��Դ���ش��������⣺
(1)д������ʽΪC6H6��һ�ֺ�̼̼��������֧���������Ľṹ��ʽ��_________��
(2)��֪1��3-������ϩ(![]() )��ȥ2 mo1H ��ɱ��ų���������1��3-������ϩ_____________(�����ȶ����������ȶ���)��
)��ȥ2 mo1H ��ɱ��ų���������1��3-������ϩ_____________(�����ȶ����������ȶ���)��
(3)���Ŀ�����ʽ���ܽ��͵���ʵ��______(����ĸ)��
a.������ʹ��ˮ��ɫ
b.������ H2�����ӳɷ�Ӧ
c.�屽û�з�������ͬ���칹��
d.�ڶ��屽ֻ��һ��
(4)�ִ���ѧ��Ϊ��������̼̼֮��ļ���__________���ʱ����Ӽ��ܷ���ȡ����Ӧ���ܷ����ӳɷ�Ӧ��
(5)�ױ��DZ���ͬϵ��ױ�_________(����������������)ʹ���Ը��������Һ��ɫ���ױ��������ڼ��������������������ױ��ķ�Ӧ����ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ������װ��(���ּг�������ʡ��)����ȡ1��2-�������顣����˵����ȷ����( )
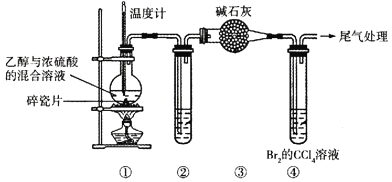
��֪����ƿ�з�Ӧ���ݳ���������Ҫ��CH2=CH2��������SO2��CO2��H2O(g)��
A.�������Ҵ���Ũ����Ļ����Һ��ʱ�����Ҵ�ע��Ũ�����в�����
B.�ڵ��Թ��п�ʢ������KMnO4��Һ�Գ�ȥSO2
C.���е�Br2����ȫ����ϩ�ӳɵ������ǣ���Һ�ɳ�ɫ��Ϊ��ɫ
D.���÷�Һ©���Ӣܷ�Ӧ��Ļ�����з����1��2-�������鲢����CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��5.6g����Ͷ�뵽ʢ��100mL2molL-1ϡ������ձ��У�2minʱ���۸պ��ܽ�(�ܽ�ǰ����Һ����仯���Բ���)�����б�ʾ�����Ӧ��������ȷ���ǣ� ��
A. v(H2SO4)��0.5mol (Lmin)-1B. v(H2SO4)��1 mol (Lmin)-1
C. v(Fe)��0.5mol (Lmin)-1D. v(FeSO4)��1mol (Lmin)-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ����Դ�ḻ���ڷ�ˮ�����Һ�о��и��ߵ����ӵ����ʵ��ŵ㡣һ�ּ����ӵ�صĹ���ԭ����ͼ��ʾ����֪�õ�ظ�����KC24-KC16-KC8֮��仯��������K2MnFe(CN)6-KMnFe(CN)6-MnFe(CN)6֮��仯������˵������ȷ���ǣ� ��
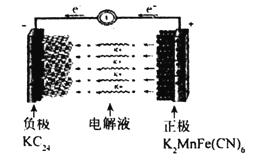
A.��ͼ��ʾΪ�����ӵ�صķŵ����
B.�ŵ�ʱ�����ɷ�����Ӧ��2KC8-e-=KC16+K+
C.���ʱ������ӦʽΪK2MnFe(CN)6-e-=KMnFe(CN)6+K+
D.�����ǰ������������ͬ������ʱÿת��0.lmole-�����������������������7.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A.��ҵ��������Ĺ�����ʹ�ù���������������߶��������ת����
B.��Ӧ2HI(g)![]() H2(g)��I2(g) ��ƽ�����С��Ӧ������������������ɫ����
H2(g)��I2(g) ��ƽ�����С��Ӧ������������������ɫ����
C.�ϳɰ�����ͨ������20 MPa��50 MPaѹǿ�������ԭ�ϵ�������
D.��HCl��Һ��������ˮϴ��AgCl�����Լ��ٳ�����ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������ȼ�����ʾ��ͼ���¡��õ���ܷ�ӦΪ��PbSO4(s)+2LiCl+Ca(s)= CaCl2(s)+ Li2SO4+Pb(s) ������˵������ȷ����
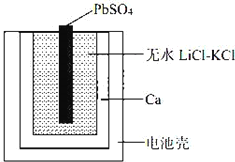
A. Ca�缫����������Ӧ
B. �����ĵ缫��Ӧ��Ca(s)+2Cl����2e��= CaCl2(s)
C. ���� LiCl �� KCl ˮ��Һ������ˮ LiCl��KCl
D. ����ˮLiCl��KCl������������ں��ز��ܹ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com