
����Ŀ������������
��1��ijʵ��С��ͬѧ��������ʵ�飬�Լ��黯ѧ��Ӧ�е������仯��ʵ���з��֣���Ӧ����е��¶����ߣ����е��¶Ƚ��ͣ��ɴ��ж�����������ķ�Ӧ��___________�ȷ�Ӧ��Ba��OH��28H2O��NH4Cl�ķ�Ӧ��________________________�ȷ�Ӧ����Ӧ����___________________________����١��ڡ����������仯����ͼ2��ʾ��

��2��Ϊ����֤Fe3+��Cu2+������ǿ��������װ���ܴﵽʵ��Ŀ����_________������ţ���

��3����CH4��Ƴ�ȼ�ϵ�أ��������ʸ��ߣ�װ����ͼ4��ʾ��a��bΪ���̼�������缫���ͨ���飨��A��B������缫��ӦʽΪ_____________________ ��

��4����ͼ5��ij��ѧ��ȤС��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�ã���ش��������⣺
�ٵ��缫aΪAl���缫bΪCu���������ҺΪϡ����ʱ��д����ԭ��������ĵ缫��ӦʽΪ___________________________ ��
�ڵ��缫aΪAl���缫bΪMg���������ҺΪ����������Һʱ����ԭ��ص�����Ϊ_______����ԭ��صĸ�����ӦʽΪ_____________________________��
���𰸡��� �� �� �� A��CH4��8e��+10OH��=CO32��+7H2O 2H++2e���TH2�� Mg Al+4OH����3e��=AlO2��+2H2O
��������
(1)��ѧ��Ӧ��,�¶�����,��Ӧ�������¶Ƚ�����Ӧ������ͼ2�з�Ӧ������������������������,�÷�ӦΪ���ȷ�Ӧ,�ݴ˽��н����
(2)��֤Fe3+��Cu2+������ǿ��,��ԭ�����,ͭ����������������Ľ�����ǽ���������,�������ҺΪ�����Ե�������
(3)���ݵ�������֪,AΪ������BΪ����,ȼ�ϵ����ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ����,����ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ��
(4)��Al��Cu��ϡ���ṹ�ɵ�ԭ���,����Al������,����CuΪ����,�����������ӵõ�����,������Alʧȥ������
��Al��Mg��NaOH��Һ���ɵ�ԭ�������AlΪ������MgΪ����,������Alʧȥ����,������ˮ�е������ӵõ��������Դ��������
(1)ͨ��ʵ����,��Ӧǰ����ձ��е��¶�����,��Al������ķ�Ӧ�Ƿ��ȷ�Ӧ,���ձ��е��¶Ƚ���,��Ba��OH��28H2O��NH4Cl�ķ�Ӧ�����ȷ�Ӧ������ͼ2���ݿ���֪��,�÷�Ӧ��,��Ӧ������������������������,��÷�ӦΪ���ȷ�Ӧ,�ɱ�ʾ��Ӧ�ٵ������仯����ˣ�������ȷ���ǣ��ţ� ���� �� ��
(2)��֤Fe3+��Cu2+������ǿ��,��ԭ�����,ͭ����������������Ľ�����ǽ���������,�������ҺΪ�����Ե����Σ�
��������������Cu������,��ط�ӦʽΪFe+2Fe3+=3Fe2+,������֤Fe3+��Cu2+������ǿ��,�ʴ���
����ͭ����������������,��ط�ӦʽΪCu+2Fe3+=2Fe2++ Cu2+������֤Fe3+��Cu2+������ǿ��,����ȷ��
�����������ۻ�����,Cu����������������,��ط�ӦʽΪ: Cu+4H++2NO3-=Cu2++2NO2��+2H2O��������֤Fe3+��Cu2+������ǿ�����ʴ���
��������������ͭ������,��ط�ӦʽΪ: Fe+ Cu2+= Cu2++ Fe2+��������֤Fe3+��Cu2+������ǿ�����ʴ���
��ˣ�������ȷ����:�ڡ�
(3)���ݵ�������֪,AΪ������BΪ����,ȼ�ϵ����ͨ��ȼ�ϵĵ缫Ϊ������ͨ���������ĵ缫Ϊ����,����A��ͨ�����,����ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ,�缫��ӦʽΪCH4��8e��+10OH��=CO32��+7H2O ��
��ˣ�������ȷ����:A��CH4��8e��+10OH��=CO32��+7H2O��
(4)��Al��Cu��ϡ���ṹ�ɵ�ԭ���,����Al������,����CuΪ����,�����������ӵõ�����,������Alʧȥ����,������ӦΪ2H++2e���TH2����
��ˣ�������ȷ������2H++2e���TH2����
��Al��Mg��NaOH��Һ�ɹ���ԭ���,AlΪ����,MgΪ����,������Alʧȥ����,������ˮ�е������ӵõ�����,����������ӷ�ӦΪAl+4OH����3e��=AlO2��+2H2O��
��ˣ�������ȷ���ǣ�Mg��Al+4OH����3e��=AlO2��+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������ˮ�ܿ�[��Ҫ�ɷ�ΪCo2O3��Co(OH)3����������Fe2O3��Al2O3��MnO��]��ȡCoCl2��6H2O�Ĺ����������£�
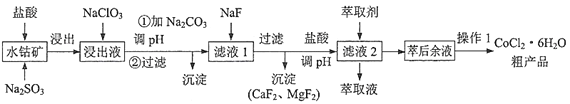
��֪��������Һ���е���������Ҫ��H+��Co2+��Fe2+��Al3+��Mn2+��Ca2+��Mg2+��
�����������ӿ�ʼ��������ȫ������pH���±�

��CoCl2��6H2O�۵�86����������ˮ�����ѵȣ��������ȶ���������110~120��ʱʧȥ�ᾧˮ�����ˮ�Ȼ��ܡ�
(1)д��Co2O3��Na2SO3�����ᷴӦ�����ӷ���ʽ______________________��
(2)����NaClO3��Ŀ����______________________���������NaClO3���������ж����壬��������___________(�ѧʽ)
(3)Ϊ�˳�ȥFe3+��Al3+�����Na2CO3��pH����pHӦ���Ƶķ�ΧΪ_____________________.
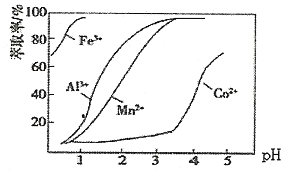
(4)����ȡ����Ŀ����___________��������������ȡ���е���ȡ����pH�Ĺ�ϵ��ͼ���ݴ˷���pH����ѷ�ͼΪ___________(����ĸ���)��
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)CoCl2��6H2O���ü�ѹ��ɷ���ɣ�ԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʒ������Ϊ������������������ҽҩ���ܼ����ϳɦ���Ʒ��G��·��֮һ����:

��֪��
��ش��������⣺
��1��A���������ŵ�������_____��
��2��B�ķ���ʽΪ_____��д��ͬʱ��������������B����״ͬ���칹��Ľṹ��ʽ��_______________��
�� �˴Ź���������2�����շ� �� �ܷ���������Ӧ
��3�� B �� C��E �� F�ķ�Ӧ���ͷֱ�Ϊ_____��_____��
��4��C �� D�Ļ�ѧ����ʽΪ_____��
��5�� ͨ�������µķ�Ӧ������E��F��G���Լ���_____��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ���������ֵΪNA������˵����ȷ����
A.1molS������Fe��Ӧ��ת�Ƶĵ�����Ϊ3NA��
B.1.5 mol NO2������H2O��Ӧ��ת�Ƶĵ�����Ϊ2NA��
C.���³�ѹ�£�46 g��NO2��N2O4������庬�е�ԭ����Ϊ3NA��
D.100 ml 0.10mol /L�İ�ˮ�У���NH3��H2O ����0.01NA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ����Ч�ɷ�Ϊ![]() ��������������Ư�ף�����ʵ������ķ�������ȷ����
��������������Ư�ף�����ʵ������ķ�������ȷ����
ʵ����� | ��
| �� | ��
|
ʵ������ | ��Ϻ���Һ�� | ��Ϻ���Һ | ��Ϻ���Һ |
A. �Ա�ʵ��ٺ͢ڣ�������ɫѸ����ȥ��ԭ���Ƿ����˷�Ӧ![]()
B. ʵ����в�����������![]() ����
����![]() �ֽ�õ���
�ֽ�õ���![]()
C. �Ա�ʵ��ںۣ͢���Һ��![]() ���ܻ�Ӱ��
���ܻ�Ӱ��![]() �������Ի�
�������Ի�![]() �Ļ�ԭ��
�Ļ�ԭ��
D. ������������84������Һ��Ư��Ч��������Ҫ���ص����ʵ�![]() ���ܰ�ȫʹ��
���ܰ�ȫʹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��״���£�1.204��1023���������ӵ������________L��
(2)��״���£�ij������ܶ�Ϊ1.25 g��L��1������Ħ������Ϊ________��
(3)��4.6 g��Ͷ��������ˮ�У�����NaOH������Ϊ______g������H2������ڱ�״����Ϊ____________��
(4)400 mLijŨ�ȵ�NaOH��Һǡ����11.2 L Cl2(��״��)��ȫ��Ӧ������NaClO�����ʵ���Ϊ________��ԭNaOH��Һ���ʵ���Ũ��Ϊ_________________��
(5)�ڱ�״���£�CO��CO2�Ļ�����干17.92 L������Ϊ28.8 g����������������ʵ���֮��Ϊ____________mol������CO2Ϊ________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڸ�����һ����̼�ɽ���������ԭΪ������
��֪����C(s)��O2(g)===CO2(g)����H1����393.5 kJ��mol��1
��CO2(g)��C(s)===2CO(g)����H2����172.5 kJ��mol��1
��S(s)��O2(g)===SO2(g)����H3����296.0 kJ��mol��1
��д��CO��SO2��Ӧ���Ȼ�ѧ����ʽ__________________________
��2����2 L�̶�������ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��_______________________����֪��K300��>K350������÷�Ӧ��______��Ӧ������ȡ������ȡ�����
����ͼ��ʾNO2�ı仯��������__________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��__________��

����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬ��ͬѹ�µ�������CO��CO2������������ȷ����(����)
A. ���֮��Ϊ2��1 B. ���֮��Ϊ7��1
C. ����ԭ����֮��Ϊ22��21 D. �ܶ�֮��Ϊ11��7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԷϾ�Ǧ�����еĺ�Ǧ���ϣ�Pb��PbO��PbO2��PbSO4��̿�ڵȣ���H2SO4Ϊԭ�ϣ��Ʊ��ߴ�PbO��ʵ��Ǧ���������á��乤���������£�

��1��Ǧ��̼��ͬ��Ԫ�أ��ұ�̼��4�����Ӳ㣬��Ǧλ��Ԫ�����ڱ���____����___��
��2�����̢��У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4�����ӷ���ʽ��________________��
��3�����̢��У�Fe2+�����̿ɱ�ʾΪ��
i��2Fe2++ PbO2+4H++SO42��2Fe3++PbSO4+2H2O ii: ����
�� д��ii�Ļ�ѧ����ʽ��_________________________��
�� �����ʵ�鷽����֤ʵ���������̡���ʵ�鷽������������
a.���ữ��FeSO4��Һ�м���__________��Һ����Һ����ɫ�仯���ټ�������PbO2����Һ��Ϊ________ɫ��
b.��a�õ�����Һ�м���___________________,��Һ�ָ�ԭ������ɫ��
��4������II�й��˲�������Ҫ�IJ���������__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com