
NA代表阿伏伽德罗常数,下列说法正确的是
A. 1.4g乙烯和丙烯混合气体中含有C—H键的数目为0.2NA
B. 0.10molFe粉与足量水蒸气反应生成的H2分子数为0.10NA
C. 标准状况下,11.2LCO2与足量Na2O2反应,转移的电子数为NA
D. 若将1mol氧化铁完全转化为氢氧化铁胶体,则分散系中胶体粒子数为NA
科目:高中化学 来源:2016-2017学年黑龙江省高一下学期开学考试化学试卷(解析版) 题型:实验题
Ⅰ.实验室需要配制0.1 mol·L-1NaOH溶液500mL。
(1)根据计算用托盘天平称取的质量为__________g。在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 _____________。
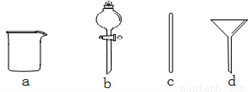
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是(_____)
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
II.向浓度相等、体积均为100 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
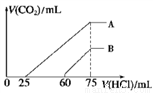
(4)①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2 的最大体积是_________mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
III.某学生用 Na2CO3和 NaHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
实验序号 | ① | ② | ③ |
盐酸体积/mL | 50 | 50 | 50 |
固体质量/g | 4.11 | 8.22 | 16.44 |
生成气体体积/L(标况) | 1.008 | 2.016 | 2.016 |
(5)原混合物样品中 n(Na2CO3)∶n(NaHCO3)=____________ , 盐酸的物质的量浓度为________mol/L ,实验③反应后,至少需继续加入_____mL的该盐酸溶液才能把混合物全部反应。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:
N2O4(g) 2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2
②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变
⑥烧瓶内气体的颜色不再加深
⑦烧瓶内气体的平均相对分子质量不再变化
⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧ C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:选择题
室温下向10ml 0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是
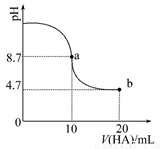
A. a点所示溶液中c(A-)+c(HA)=0.1mol·L-1
B. b点所示溶液中c(HA)>c(A-)
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. a、b两点所示溶液中水的电离程度a>b
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:选择题
下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是
A. 氧化镁中混有氧化铝 B. 氯化铝溶液中混有氯化铁
C. 氯化亚铁溶液中混有氯化铜 D. 氧化铁中混有二氧化硅
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三下学期第一次月考理科综合化学试卷(解析版) 题型:推断题
青蒿素是从黄花蒿中提取的一种无色针状晶体,双氢青蒿素是青蒿素的重要衍生物,抗疟疾疗效优于青蒿素,请回答下列问题:
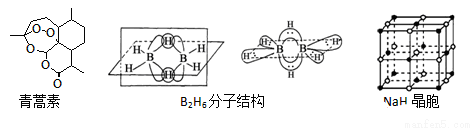
(1)组成青蒿素的三种元素电负性由大到小排序是__________,画出基态O原子的价电子排布图__________。
(2)一个青蒿素分子中含有_______个手性碳原子。
(3)双氢青蒿素的合成一般是用硼氢化钠(NaBH4)还原青蒿素.硼氢化物的合成方法有:
2LiH+B2H6=2LiBH4; 4NaH+BF3═NaBH4+3NaF
①写出BH4﹣的等电子体_________(分子、离子各写一种);
②B2H6分子结构如图,2个B原子和一个H原子共用2个电子形成3中心二电子键,中间的2个氢原子被称为“桥氢原子”,它们连接了2个B原子.则B2H6分子中有______种共价键,B原子的杂化方式为________ ;
③NaBH4的阴离子中一个B原子能形成4个共价键,而冰晶石(Na3AlF6)的阴离子中一个Al原子可以形成6个共价键,原因是______________;
④NaH的晶胞如图,则NaH晶体中阳离子的配位数是_________;设晶胞中阴、阳离子为刚性球体且恰好相切,求阴、阳离子的半径比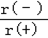 =__________。
=__________。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
W、X、Y、Z均为的短周期元素,原子序数依次增加, W的原子核外最外层电子数是次外层的2倍, X-、Y+具有相同的电子层结构, Z的阴离子不能发生水解反应。下列说法正确的是
A. 原子半径:Y>Z>X>W
B. 简单氢化物的沸点: Z>X>W
C. 最高价氧化物的水化物的酸性:W<Z<X
D. X与Y两种元素组成的化合物是离子化合物
查看答案和解析>>
科目:高中化学 来源:2017届河北省唐山市高三下学期第一次模拟考试理综化学试卷(解析版) 题型:填空题
PM2.5中的某些物质,易引发光化学烟雾污染,光化学烟雾中含有NOx、OCS、CH2=CH-CHO、HCOOH、以及光气等二次污染物。水污染程度可通过测定水体中铅、铬等重金属的含量判断。
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______(用元素符号表示),CH2=CH-CHO分子醛基中碳原子杂化方式为____________。
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_________;光气(COCl2)各原子最外层都满足8电子稳定结构,则光气分子的空间构型为_________(用文字描述);
(3)1molHCOOH中含σ键和π键数目之比为______________。
(4)基态Cr原子核外电子排布式是_______,配合物[Cr(NH3)4(H2O)2] Cl3中心离子的配体为_______。
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=______(填数字)。若两个相邻面心的Kr原子的核间距为acm,用NA表示阿伏伽德罗常数,M表示Kr的相对原子质量。该晶体的密度计算式为______ g/cm3。

查看答案和解析>>
科目:高中化学 来源:广东省2016-2017学年高一上学期期末考试化学试卷 题型:选择题
下列离子方程式书写正确的是( )
A. 用FeCl3溶液腐蚀铜线路板:Cu + Fe3+ = Cu2+ + Fe2+
B. Na2O2固体与H2O反应产生O2 :2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑
C. Ba(OH)2溶液中加入稀硫酸 Ba2+ + OHˉ + H+ + SO42-= BaSO4↓+ H2O
D. 向氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com