
100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:
N2O4(g) 2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2
②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变
⑥烧瓶内气体的颜色不再加深
⑦烧瓶内气体的平均相对分子质量不再变化
⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧ C. 只有①④ D. 只有⑦⑧
科目:高中化学 来源:2017届浙江省高三3月选考化学试卷(解析版) 题型:填空题
为了确定黄钾铁矾[KFe3(SO4)x(OH)y]的化学式,某兴趣小组设计了如下实验:

请回答:
(1)黄钾铁矾的化学式[KFe3(SO4)x(OH)y]中x=________,y=________。
(2)写出溶液B中所含溶质的化学式________。
(3)红褐色沉淀能溶于HI溶液,并发生氧化还原反应,写出该反应的离子方程式________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A. 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B. 江河入海口三角洲的形成通常与胶体的性质有关
C. 用激光笔检验淀粉溶液的丁达尔效应
D. 纳米材料属于胶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
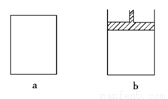
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变。在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应:2NO2 N2O4(正反应放热),则以下说法正确的是
N2O4(正反应放热),则以下说法正确的是
A. 反应起始时反应速率的关系:va<vb
B. 反应过程中反应速率的关系:va<vb
C. 两容器内反应达到平衡所需时间一定相同
D. 反应达到平衡,两容器中的NO2的转化率相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
已知:Fe2O3(s)+ C(s)===
C(s)=== CO2(g)+2Fe(s) ΔH=+234.14 kJ/mol,
CO2(g)+2Fe(s) ΔH=+234.14 kJ/mol,
C(s)+O2(g)===CO2(g)ΔH=-393.5 kJ/mol,
则2Fe(s)+ O2(g)===Fe2O3(s)的ΔH是( )
O2(g)===Fe2O3(s)的ΔH是( )
A. -824.4 kJ/mol B. -627.6 kJ/mol
C. -744.7 kJ/mol D. -169.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c(NH4+)=c(Cl-) ⑤c(NH4+)<c(Cl-)正确的是( )
A. ①⑤ B. ③④ C. ②⑤ D. ②④
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:实验题
工业上用某矿渣(含有Cu2O、Al2O3,Fe2O3、SiO2)制取铜的操作流程如下:
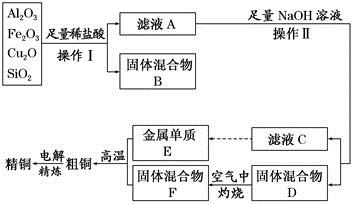
已知:Cu2O+2H+= Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为 ;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有 (填仪器名称)。
(2)滤液A中铁元素的存在形式为 (填离子符号),生成该离子的离子方程式为 ,检验滤液A中存在该离子的试剂为 (填试剂名称)。
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为 。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH= 。
(5)利用电解法进行粗铜精炼时,下列叙述正确的是 (填代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
(6)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→ →过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,说出主要操作方法,不必描述操作过程的细节)
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:选择题
NA代表阿伏伽德罗常数,下列说法正确的是
A. 1.4g乙烯和丙烯混合气体中含有C—H键的数目为0.2NA
B. 0.10molFe粉与足量水蒸气反应生成的H2分子数为0.10NA
C. 标准状况下,11.2LCO2与足量Na2O2反应,转移的电子数为NA
D. 若将1mol氧化铁完全转化为氢氧化铁胶体,则分散系中胶体粒子数为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:实验题
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 112 | 难溶 |
实验步骤:
在A 中加入4.40g异戊醇、6.00g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯4.55g。
请回答下列问题:
(1)仪器B的名称是_____;B中冷却水是从_____(填“下口”或“上口”)流进的。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的操作是_____________________。
(3)在洗涤、分液操作中,第二次洗涤,用饱和碳酸氢钠溶液洗涤的主要目的是_______,不能用NaOH溶液洗涤的原因是___________。第二次洗涤后,充分振荡,然后静置,待分层后,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)在蒸馏操作中,仪器选择及安装都正确的是下图中的_____(填字母标号),若从130℃ 便开始收集馏分,会使实验的产率______(填“偏高”、“偏低”或“无影响”)。

(5)水的沸点为100℃,比乙酸异戊酯低42℃ ,但仍要先加入MgSO4后过滤再蒸馏,而不是直接蒸馏。结合题中信息分析,下列说法正确的是______(填字母)。
A.水可能会与乙酸异戊酯形成一种“恒沸溶液”(在溶液的某一组成时,在某温度下,混合液同时汽化或同时冷凝),不能进一步提纯,所以要先用MgSO4干燥
B.在加入MgSO4后如不先过滤就蒸馏,加热时硫酸镁的结晶水合物又会脱水
C.如不先用MgSO4吸收水分,蒸馏时水先被蒸出,浪费能源和延长蒸馏时间
D.本实验中要乙酸过量,而不是异戊醇过量,可能的原因是异戊醇比乙酸价格贵;另外异戊醇过量时,异戊醇与乙酸异戊酯沸点相近(小于30℃),蒸馏时完全分离困难
(6)将乙酸异戊酯中的异戊醇除去,是在哪个步骤中除去的______(填字母)。
A.在第一次水洗和后面的分液中除去的
B.在第二次用饱和碳酸氢钠溶液洗涤和后面的分液中除去的
C.在“过滤”中除去的
D.由于本实验中加入过量乙酸,异戊醇已经反应完全,所以不需除杂(异戊醇)了
E.在最后的“蒸馏”步骤中除去的
(7)产物乙酸异戊酯的产率是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com