
| A. |  海水蒸馏 | B. | 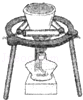 钾在空气中的燃烧 | ||
| C. | 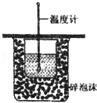 测定中和热 | D. |  牺牲阳极的阴极保护法 |
分析 A.冷水下进上出效果好;
B.K可在坩埚中燃烧,与二氧化硅不反应;
C.图中缺少环形玻璃搅拌棒;
D.牺牲阳极的阴极保护法为原电池原理,而图中有外加电源.
解答 解:A.图中蒸馏装置,冷水应从下口进入,冷却效果好,而图中下口流出热水,则操作不合理,故A错误;
B.在坩埚中可完成K的燃烧反应,图中实验操作合理,故B正确;
C.缺少环形玻璃搅拌棒,不能测定反应的最高温度,则不能测定中和热,故C错误;
D.由外加电源可知,Zn为阳极,Fe为阴极,Fe被保护,则该方法为外加电源的阴极保护法,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离实验、中和热测定、电化学等为解答的关键,注意化学反应原理及实验装置的作用,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
 过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 试剂 | 操作方法 |
| A | 除去CH4中的C2H4 | 溴水 | 洗气 |
| B | 除去工业酒精中的水 | CaO | 蒸馏 |
| C | 除去苯中的溴 | 乙醇 | 分液 |
| D | 从肥皂、甘油的混合液中分离出肥皂 | NaCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ | |
| B. | 若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ | |
| C. | 若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间不相同 | |
| D. | 平衡时Ⅰ容器的体积小于V L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

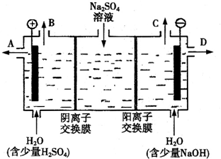
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| B. | 1 L 0.1mol•L-1氨水含有0.1NA个OH- | |
| C. | 电解饱和食盐水若产生2g氢气,则转移2NA个电子 | |
| D. | 将0.1mol氯化铁溶于1 L水中,所得溶液含有0.1NA个Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Na+、SO42-、MnO4- | B. | K+、Fe2+、SO42-、HCO3- | ||
| C. | Ba2+、K+、Al3+、Cl- | D. | Na+、Ba2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com