
̽��Ũ�ȶԻ�ѧƽ���Ӱ�죬ʵ�����£�
I����5mL 0.05mol/L FeCl3��Һ�м���5mL 0.05mol/L KI��Һ����Ӧa����ƽ����Ϊ���ȷ�
����һ�ݼ��뱥��KSCN��Һ����죨��Ӧb��������CCl4�������ã��²��Լ�dz����ɫ
������һ�ݼ���CCl4�������ã��²����Ϻ�ɫ
���ʵ�飬����˵������ȷ����
A. ��ӦaΪ��2Fe3++ 2I- 2Fe2++I2
2Fe2++I2
B. ���У���Ӧa���еij̶ȴ��ڷ�Ӧb
C. �Ƚ������ԣ����У�I2>Fe3+
D. �Ƚ�ˮ��Һ��c(Fe2+)����<��
 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ�����и�һ��ѧ�ڵ�һ�νμ�⻯ѧ�Ծ��������棩 ���ͣ������
�������������������м�����Ҫ�����ã��������й��ס���Ч���Ͷ���ɱ�������������ǽ��չ�����ơ�
��1��Cl2��H2O2��ClO2����ԭ����ΪCl������O3��1mol O3ת��Ϊ1mol O2��1mol H2O�������ʳ��������������������ʵ�����������������Ч����ߵ��� ������ţ���
A��Cl2 B��H2O2 C��ClO2 D��O3
��2��H2O2��ʱ����Ϊ��ҵ��Һ���������С���ɫ�������������ƣ��������ɿ�ҵ��Һ�е��軯���KCN���������·�Ӧʵ�֣�KCN+H2O+H2O2�TA+NH3������������A�Ļ�ѧʽΪ ��H2O2����Ϊ����ɫ���������������� ��
��3��Ư���������ƣ�NaClO2���ڳ�����ڰ����ɱ���һ�꣮������ȶ��ɷֽ⣬��Ӧ�����ӷ���ʽΪHClO2 �� ClO2��+H++Cl��+H2O��δ��ƽ�����ڸ÷�Ӧ�У�����1mol ClO2����ʱת�Ƶĵ��Ӹ���ԼΪ ��
��4����84������Һ����Ҫ�ɷ���NaClO���ͽ������Ҫ�ɷ���Ũ���ᣩ���ܻ��ã�ԭ���� �������ӷ���ʽ��ʾ���������ȼҵ�IJ������������84������Һ��д���йط�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڼ�������ʵıȽϣ�����ȷ����
A. ���ǵ�ԭ�Ӻ�����Ӳ�����˵���������������
B. �˵������Ŀɽ��˵����С�Ĵ����⻯���ˮ��Һ���û�����
C. ������ķ�Ӧ��˵���������Ӷ�Խ��Խ����
D. �ۡ��е���˵���������Ӷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��ͨ�и����߿�ȫ��ģ�⣨һ����ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼΪ1 mol SO2Cl2(g����1 mol SCl2(g����Ӧ����SOCl2(g���������仯��ʾ��ͼ,��֪E1=xKJ/mol��E2=yKJ/mol�������й�˵����ȷ����

A. ���ڷ�Ӧ��ϵ�м��˴�����E1����
B. ���ڷ�Ӧ��ϵ�м��˴���, ��H��С
C. �÷�Ӧ�Ļ�ܵ���ykJ/mol
D. 1 mol SO2Cl2 (g����1mol SCl2(g����Ӧ����SOCl2(g���Ħ�H=(x-y)kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���г�����������һ�Σ�3�£��ۺ���ϰ���ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
ijѧ��̽������ʵ��(A)��
ʵ��A | ���� | ���� |
| ���� | i�����Ⱥ���ɫ��ȥ ii����ȴ�����У���Һ�ָ���ɫ ��.һ��ʱ�����ɫ������ȥ |
��1��ʹ���۱�����������____��
��2����������i��ii��Ϊ�������������£����ȴٽ�����ˮ�⣬��ȴ��ƽ�������ƶ���
���ʵ�����£�������a��֤ʵ�÷�����������
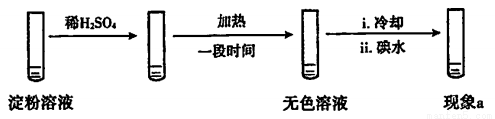
������a����____��
��3���ٴη��������Ⱥ��ʵⷢ���˱仯��ʵ�����£�
I��ȡ������ˮ����������ɫ���õ�����Һ����ӷ��������ʣ�������
������ɫ�����Һ�еμӵ�����Һ����ȴ������һֱδ����������ϡH2SO4��˲�������
�Բ������ϡH2SO4�����ã�������ӷ���ʽ�����һ�ֺ����Ľ��ͣ�______________��
��4��̽����ˮ��ɫ����Һ�ijɷ֣�
ʵ��1�������Һ��pH��5
ʵ��2��ȡ��ɫ�����Һ���������ʵ�飺
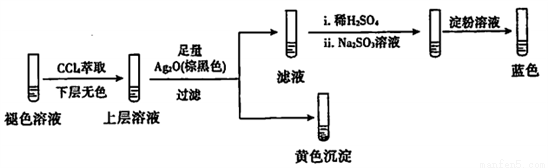
�ٲ�����ɫ���������ӷ���ʽ��____��
��Ag2O��������____________��
����������ʵ�飬�Ʋ���Һ�к��е����ʣ������ӣ�������_________��
��5����ϻ�ѧ��Ӧ���ʽ���ʵ��A������i������iii��ɫ��ȥ��ԭ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���г�����������һ�Σ�3�£��ۺ���ϰ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������г��õ�ʳ�ﴢ�淽���У��������ʲ���������Ӧ����
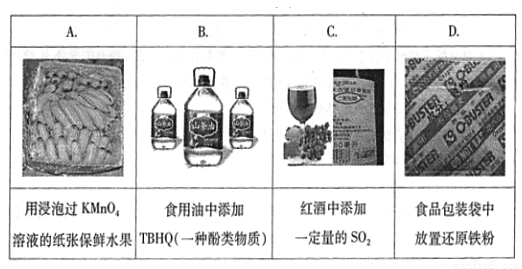
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�ڵ�һ���¿���3�£���ѧ�Ծ��������棩 ���ͣ�ѡ����
200 mL 1 mol/L���Ȼ�����Һ�м���һ�������2 mol/L��NaOH��Һ�����ղ���7.8 g������������NaOH��Һ����������ǣ� ��
�� 350 mL �� 90 mL �� 150 mL ��200 mL
A. ֻ�Т� B. �٢� C. �ڢ� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���Ĵ�ʡ�ɶ��б���У��2016-2017ѧ���һ3���¿���ѧ�Ծ� ���ͣ������
����A��B��C��D��E��F���ֶ�����Ԫ�أ�����B��C��D��E����Ԫ���ڻ�ѧ��Ӧ�о����γɼ����������ӣ���B��C��D���Ӿ�����ͬ�ĵ��Ӳ�ṹ����֪��
��A���γ�������������Ԫ�أ�F��Aͬ���壻
��C���⻯�����G�Ǿ���10���ӵ������ҿ��Է�����ͼת����

��E��D��ͬ����Ԫ�أ�
��B��D���γɸ�����Ϊ1��1��2��1�����ӻ�����X��Y��
��ش��������⣺
(1)B��D�γ����ӻ�����Y����Ư���ԣ�д��Y�ĵ���ʽ______���û������Ԫ��A�����������O��Ӧ�Ļ�ѧ����ʽΪ��__________��һ������Y��O��Ӧ��õ��Ĺ������ʣ���ǡ���뺬400 mL 2 mol/L��ϡ���ᷴӦ�����ռ���0.25 mol���壬��ù������ʵ����Ϊ________�������ʵ�����ʾ����
(2)G����ļ��鷽��Ϊ_________��13.44 L����G(��״���²ⶨ��������ͼת����ʽ���Ի��M���ʵ����ֱ�Ϊ__________mol��
(3)ij��ѧ��ȤС����������ͼװ��֤��A��C��F����Ԫ�����ʵĵݱ��ԣ����м�װ������ƿ�������Լ�Ϊʯ��ʯ��

�ټ�װ���з�����Ӧ�����ӷ���ʽΪ________________��
����װ����Ӧ���ӵ��Լ�Ϊ______________��
�۱�װ���п��ܷ�����ʵ������Ϊ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�Э����2017�������19�죨3�£��������ۻ�ѧ�Ծ� ���ͣ������
ij��ѧ����С��ͨ��ʵ��̽��NO�ܷ���Na2O2��Ӧ�Լ���Ӧ��IJ����СС��ͬѧ�������ͼ��ʾװ��(�г������������õ��齺�ܾ���ʡ��)��
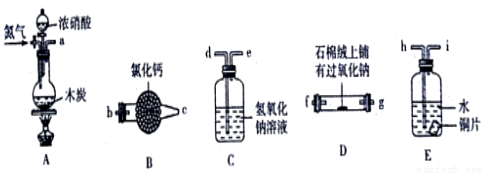
����������֪:��NO�Dz������������2NO2+2NaOH =NaNO3+NaNO2+H2O��
�ش��������⣺
��1��д��ľ̿��Ũ���ᷴӦ�Ļ�ѧ����ʽ��________________��
��2��Ϊ�����ʵ�飬ѡ����ͼ�е�װ�ã�������˳��Ϊa��_______(������������Сд��ĸ��ʾ)����ͬѧ��Ϊ��װ�ô���ȱ�ݣ����ȱ����______________��
��3�����Ӻ�������_____________��װ��ҩƷ��Ҫͨ��һ��ʱ��ĵ������ڵ���Ũ���ᣬ��ȼ�ƾ��ƣ�ͨ�뵪������ҪĿ����_______________��
��װ��E��������________________����˵��NO��Na2O2������Ӧ��ʵ��������_____________��
��5��̽��NO��Na2O2��Ӧ�IJ��
����1������ֻ��NaNO3������2��_________________��
����3������ΪNaNO3��NaNO2�Ļ���
Ϊ��֤��Ӧ�����С��ͬѧȷ��ȡ��Ӧ��Ĺ���3.50g������в���ȴ�������ˮ���100.00mL��Һ��ȡ10.00mL��Һ����ƿ�У���0.1000mol��L-1KMnO4��Һ(�����ữ)�ζ���������KMnO4��Һ20mL���ζ������з�����Ӧ�����ӷ���ʽΪ___________________����Ӧ������NaNO2����������Ϊ_____(������λ��Ч����)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com