(2010?启东市模拟)在水溶液中高价金属离子如:Fe
3+、Al
3+等会发生强烈水解,同样二价金属离子如Cu
2+、Pb
2+、Zn
2+等离子在一定的pH范围内也可以水解.金属氢氧化物的沉淀直接受溶液pH的控制,利用这一方法可以除去工业污水中的某些金属离子.下图是Zn(OH)
2的在某温度时的沉淀区域曲线图
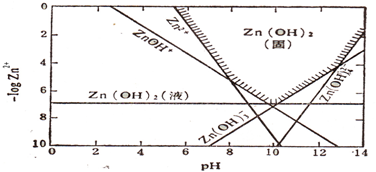
请回答下列问题:
(1)向一定浓度的Zn
2+的溶液中加入足量的NaOH固体,下列说法正确的是
D
D
A、一定产生沉淀 B、先产生沉淀,后沉淀消失
C、一定不产生沉淀 D、可能不产生沉淀
(2)当pH=6、c(Zn
2+)=0.01mol?L
-1,Zn
2+主要存在形式为
ZnOH+
ZnOH+
、
Zn(OH)2液体
Zn(OH)2液体
.
(3)向c(Zn
2+)=1×10
-5mol?L
-1的溶液中加入固体NaOH到pH=10和pH=13,写出有关反应的离子方程式:①
Zn2++2OH-═Zn(OH)2↓
Zn2++2OH-═Zn(OH)2↓
;②
Zn2++4OH-═Zn(OH)2-4
Zn2++4OH-═Zn(OH)2-4
(4)已知该温度下的Ksp[Zn(OH)
2]=1×10
-17,计算:当溶液中的c(Zn
2+)=1×10
-5mol?L
-1,向溶液中加入NaOH固体,产生沉淀的pH,并对照该图判断是否真的产生沉淀?原因可能是什么?

 快捷英语周周练系列答案
快捷英语周周练系列答案 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是( )
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是( )