
【题目】下列物质不能通过化合反应得到的是
A. Fe(OH)2 B. Fe(OH)3 C. FeCl2 D. FeCl3
科目:高中化学 来源: 题型:
【题目】某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
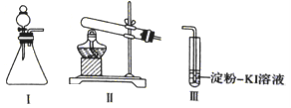
供选试剂:30%H2O2溶液、0.lmol/LH2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如下
操作 | 现象 | |
甲 | 向I的锥形瓶中加入_____,向I的_________中加入30%H2O2溶液,连接I、. Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1 mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式是___________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是__________________。为进一步探究该条件对反应速率的影响,可采取的实验措施是___________________________。
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝。学生将I中产生的气体直接通入下列__________ (填字母)溶液,证明了白雾中含有H2O2。
A.酸性 KMnO4 B. FeC12 C. Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O==2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应,3I2+6OH-==5I-+IO3-+3H2O造成的。请设计实验证明他们的猜想是否正确:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,实验现象与结论均正确的是( )

选项 | 实验试剂 | 实验现象 | 实验结论 | ||
a | b | c | |||
A | 浓氨水 | 碱石灰 | FeCl2溶液 | 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 | 氨气具有氧化性 |
B | 稀硫酸 | FeS | AgCl悬浊液 | 悬浊液由白色变为黑色 | Ksp(AgCl)>Ksp(Ag2S) |
C | 浓硝酸 | 铜 | BaSO3悬浊液 | 悬浊液变澄清 | +4价硫具有还原性 |
D | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)D、E两种元素的单质反应生成的两种离子化合物分别是________、___________。
(2)化学组成为BDF2的电子式为:_______,A、C、F三种元素形成的化合物CA4F为_________化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:_______________________________。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是_________________ (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性_________于F(填“强”或“弱”),并用化学方程式证明上述结论_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淮南是我国重要的煤炭生产基地,通过煤的气化和液化,能使煤炭得以更广泛的应用。
I.工业上先将煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
(1)向2L恒容密闭容器中充入CO和H2O(g),800℃时测得部分数据如下表。
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
则从反应开始到2min时,用H2表示的反应速率为_________________;该温度下反应的平衡常数K=___________________(小数点后保留1位有效数字)。
(2)相同条件下,向2L恒容密闭容器中充入1molCO、3mol H2O(g)、2molCO2(g)、2mo1 H2(g),此时v正________v逆(填“>” “<” 或 “=”)。
Ⅱ.一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g)△H=﹣105kJmol﹣1.向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如右图中Ⅰ、Ⅱ、Ⅲ曲线所示:
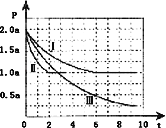
(1)Ⅱ和Ⅰ相比,改变的反应条件是______.
(2)反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=______.
(3)反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=______.
(4)比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”),判断的理由是_________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1 mol苯甲酸在浓H2SO4存在下与足量乙醇反应可得1 mol苯甲酸乙酯
B. 对苯二甲酸(![]() )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维(
)与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维(![]() )
)
C. 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种
D. ![]() 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃沸点由高到低顺序正确的是( ) ①CH4 ②C3H8 ③C5H12 ④C8H18 ⑤C12H26 .
A.①②③④⑤
B.⑤④③②①
C.⑤③④②①
D.③④⑤②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是 ( )。
A. 天然气的主要成分为CH4
B. 1 mol Cl2与1 mol CH4恰好完全反应,则转移的电子总数为2 NA
C. 已知CH4+H2O![]() CH3OH+H2该反应的有机产物是无毒物质
CH3OH+H2该反应的有机产物是无毒物质
D. CH4的二氯代物只有一种,此事实可说明CH4为正四面体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
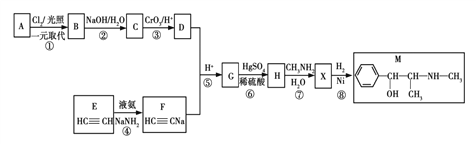
已知:Ⅰ.芳香烃A的相对分子质量为92
Ⅱ.R—CH2OH![]() RCHO
RCHO
Ⅲ.R1—CHO+R—C![]() CNa
CNa![]()
![]()
Ⅳ.![]()
![]()
![]()
Ⅴ.![]()
![]()
![]()
请回答下列问题:
(1)D的名称是___________;G中含氧官能团的名称是___________。
(2)反应②的反应类型为___________;A的结构简式为___________。
(3)写出反应⑦的化学方程式______________________。
(4)X分子中最多有___________个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物有___________种。其中,核磁共振氢谱上有4组峰,且峰面积之比为1︰1︰2︰6的有机物的结构简式为______________________。
(6)已知:![]()
![]()
![]() 。仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
。仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线______________________。
的路线______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com