
将二氧化碳通入下列物质的溶液中不与其反应的是( )
①Na2CO3 ②Na2SiO3 ③NaAlO2 ④Ca(ClO)2 ⑤ CaCl2 ⑥CaCO3
A.①③④⑤ B.①和⑤ C.只有① D.只有⑤
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:阅读理解
 (2009?厦门二模)纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列三种实验方案进行探究.请填空:
(2009?厦门二模)纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列三种实验方案进行探究.请填空:| 加热 |
| ||
| ||

| 氯化钙溶液 |
| 106m2 |
| m1 |
| 106m2 |
| m1 |
| 硫酸 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
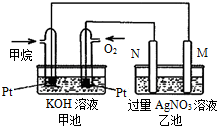 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.
天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:
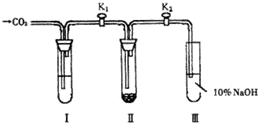 为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,课题研究小组的同学们设计了如图所示的实验装置,分别进行甲、乙两次实验:
为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,课题研究小组的同学们设计了如图所示的实验装置,分别进行甲、乙两次实验:查看答案和解析>>
科目:高中化学 来源:英德中学2007届高三化学第二轮复习专题强化训练9 题型:058
我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出贡献.他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气和二氧化碳为原料制得NaHCO3,进而生产出纯碱.
(1)某研究性学习小组的同学,模拟“侯氏制碱法”提出下列三种制备NaHCO3的实验方案.经过讨论,大家一致认为方案2较合理,请说明方案3的不足之处是________.
方案1:分别将二氧化碳和氨气通入饱和食盐水中;
方案2:将二氧化碳通入含氨的NaCl饱和溶液;
方案3:将氨气通入含二氧化碳的NaCl饱和溶液中.
(2)根据方案2,某同学设计了如下实验步骤和装置图:

步骤1:配制含氨的饱和食盐水.在100 mL的锥形瓶中加入20 mL氨水(体积比1:1),再加入8 g食盐,塞紧橡皮塞,振荡几分钟,过滤除去不溶物,得到含氨的饱和食盐水.
步骤2:制备碳酸氢钠.按图组装实验装置,先检查装置的气密性,再向各仪器中加入相应的试剂,开始制备碳酸氢钠.实验过程中,需要控制温度在30℃-35℃(大于35℃时NH4HCO3会分解)和二氧化碳的通入速度(以出现能数得清的连续气泡为好).反应结束后,把锥形瓶浸入冷水中,使较多的晶体析出,过滤、洗涤.
请回答下列问题:
①为控制反应温度在30℃~35℃,应采用的操作方法是________.
②装置B中试剂是________,它的作用为________.
③装置C中的化学方程式为________.
④检验步骤2中所得晶体是碳酸氢钠而不是氯化钠的的实验方法和现象是________.
⑤请你设计一个简单的实验方案证明纯碱溶液呈碱性是由CO32-引起的.
答:________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com