
【题目】某实验小组用0.50mol·L-1 NaOH溶液和0.50mol·L-1硫酸溶液进行反应热的测定。
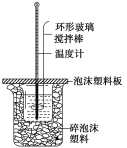
(1)写出该反应的热化学方程式[生成1 molH2O(l)时的反应热为-57.3 kJ·mol-1]:___。
(2)取50 mLNaOH溶液和30 mL 硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
温度 次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ___ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸溶液的密度都是1.0g·mL-1,中和后生成溶液的比热容c=4.18J/(g·℃)。则生成1 mol H2O(l)时的反应热ΔH=___(取小数点后一位)。
③上述实验数值结果与-57.3kJ·mol-1有偏差,产生偏差的原因不可能是(填字母)___。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
【答案】H2SO4(aq)+2NaOH(aq)===Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1 4.0 -53.5 kJ·mol-1 b
【解析】
(1)强酸强碱的中和热为-57.3kJ/mol,中和热是强酸和强碱的稀溶液完全反应生成1mol水放出的热量,稀硫酸和稀氢氧化钠溶液反应的热化学方程式为:12H2SO4(aq)+NaOH(aq)=12Na2SO4(aq)+H2O(l) △H=-57.3 kJmol-1;
(2)①4次温度差分别为:4.0℃,6.1℃,3.9℃,4.1℃,其中第2组数据相差较大,舍去,用其他3组数据计算,温度差平均值=4.0℃+3.9℃+4.1℃3=4.0℃;
②50mL0.50mol/L氢氧化钠与30mL0.50mol/L硫酸溶液进行中和反应生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为:80ml×1g/ml=80g,温度变化的值为△T=4℃,则生成0.025mol水放出的热量为Q=mc△T=80g×4.18J/(g℃)×4.0℃=1337.6J,即1.3376kJ,所以实验测得的中和热△H=-1.3376kJ÷0.025mol=-53.5kJ/mol;
(3)a、装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小;
b、量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,放出的热量偏高,中和热的数值偏大;
c、尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,不允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,会导致热量散失,数据偏小;
d、温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高,测得的热量偏小,中和热的数值偏小;
所以会导致偏大的是b,故选b。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3L的密闭容器中,发生反应:CO(g)+2H2(g)![]() CH3OH(g),在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是
CH3OH(g),在不同温度下甲醇的物质的量随时间的变化如图所示。下列叙述正确的是

A. 平衡常数K(300 ℃)<K(500 ℃)
B. 在其他条件不变时,压缩处于E点的体系体积,氢气浓度增大
C. 300 ℃,当容器内气体密度不变时说明反应已经达到平衡
D. 500 ℃,从反应开始到平衡,氢气的平均反应速率v(H2)=![]() mol·L1·min1
mol·L1·min1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molSO2和2molO2的混合气体置于体积可变的恒压容器中,在一定条件下发生如下反应2SO2(g)+ O2(g)![]() 2SO3(g) ΔH<0,该反应达平衡时,测得气体总物质的量为4.2mol,试回答:
2SO3(g) ΔH<0,该反应达平衡时,测得气体总物质的量为4.2mol,试回答:
(1)在该平衡时,n(SO3)=_____mol
(2)若起始时加入1.2molSO2、0.6molO2和xmolSO3,达到平衡时各气体体积分数与上述平衡状态相同,则x的取值范围是________
(3)若反应开始时v(逆)> v(正),达到上述平衡状态时,气体的总物质的量仍为4.2mol,则起始时n(SO3)的取值范围是______
(4)若反应过程中SO2、O2、SO3物质的量变化如图所示。则反应进行至20min时,曲线发生变化的原因是______________________(用文字表达)。10 min到15 min的曲线变化的原因可能是_________(填写编号)。

A.加了催化剂 | B.缩小容器体积 |
C.降低温度 | D.增加SO3的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述和解释均正确且有对应关系的是( )
选项 | 描述 | 解释 |
A | 84消毒液可以消灭新型冠状病毒 |
|
B | 用灼烧法鉴别纤维素和聚乙烯塑料 | 纤维素有烧焦羽毛的气味 |
C | 《易经》载有“泽中有火”上火下泽” | 燃烧的气体可能为水煤气 |
D | 《四川盐法志》记载;当煮盐近于饱和时,往卤水中点加豆汁,至渣滓皆浮聚于面 | 加豆汁除渣利用了胶粒的吸附作用 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素![]() 的原子序数依次增大,W原子的最外层电子数等于Y原子最外层电子数的2倍;四种元素形成的一种化合物的结构如图所示,该化合物的阴离子中每个原子的最外层均满足8电子稳定结构,下列说法错误的是( )
的原子序数依次增大,W原子的最外层电子数等于Y原子最外层电子数的2倍;四种元素形成的一种化合物的结构如图所示,该化合物的阴离子中每个原子的最外层均满足8电子稳定结构,下列说法错误的是( )

A.原子半径:![]() B.W与Z形成晶体的基本单元为平面结构
B.W与Z形成晶体的基本单元为平面结构
C.X与Z在自然界中均不存在游离态D.W与Y形成的化合物可作耐火材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素形成的单质和化合物在化工、材料、医学等领域应用广泛,回答下列问题:
(1)区分金刚石和无定形碳最可靠的科学方法为___________。基态C原子核外未成对电子的数目为_____________。
(2)咖啡因结构为 。
。
①咖啡因中C原子的杂化形式为_________________。
②1 mol咖啡因中所含![]() 键数目为_________________。
键数目为_________________。
③咖啡因通常在水中的溶解度较小,加入适量![]() 能增大其在水中溶解度的原因为_________________。
能增大其在水中溶解度的原因为_________________。
④CH3+(甲基正离子)的立体构型为_________________。
(3)CO、NO、H2S均为生命体系气体信号分子。其中H、C、O、S的电负性由大到小的顺序为____________;N、O、S的第一电离能由大到小的顺序为________________。
(4)干冰可用于人工降雨。其熔点低于金刚石的原因为___________;若干冰的密度为1.56 g/cm3,立方晶胞参数为0.57 nm,则每个晶胞实际占用CO2的数目为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛是制取海绵钛和氯化法钛白(二氧化钛)的主要原料,用于制造颜料和钛有机化合物以及国防上用的烟幕剂。同时也是制取航天航空工业材料——钛合金的重要原料,由钛铁矿(主要成分是FeTiO3,含有少量Fe2O3、SiO2、Al2O3等杂质),制备TiCl4等产品的一种工艺流程如下:

已知:
Ⅰ.①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe===3Fe2+、2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2O、Ti3+(紫色)+ Fe3++ H2O===2TiO2+(无色)+ Fe2++2H+;
Ⅱ.四氯化钛的熔点-25.0℃,沸点136.4℃,SiCl4的熔点-68.8℃,沸点57.6℃。
回答下列问题:
(1)用盐酸酸浸时,为使酸浸速率加快,可采取的措施是:________________(至少写2条),发生主要反应的离子方程式为:___________。
(2)废渣的成分是_______。
(3)如何检验富含TiO2+溶液中是否还含铁元素_____________。
(4)若将制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应![]() 的平衡常数K=____。
的平衡常数K=____。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_______(只要求写出一项)。
(6)要精制含少量SiCl4杂质的TiCl4,可采用的方法是_______。
(7)用TiCl4水解生成TiO2·nH2O,经过滤、水洗除去其中的Clˉ,再烘干、焙烧除去水分得到粉体TiO2.写出TiCl4水解生成TiO2·nH2O的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。

下列说法不正确的是
A.此温度下该反应的化学方程式为2A(g)+B(s)![]() 3C(g)
3C(g)
B.t4-t5阶段改变的条件为减小压强
C.B的起始物质的量为1.0 mol
D.在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+2c/3=2.4和b+c/3=1.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的最外层电子数之和是Z的2倍,X的原子半径是同周期所有主族元素中最小的,W或X的简单气态氢化物分子与![]() 具有相同的电子数。
具有相同的电子数。
下列说法正确的是( )
A.简单离子半径:![]()
B.X、Y两种元素形成的化合物水溶液呈碱性
C.Y、Z的最高正价之和与X的相等
D.W的氢化物与W的氧化物之间一定不能发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com