


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
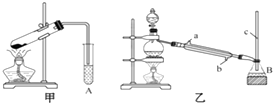 某化学兴趣小组用甲、乙两套装置(如图所示)进行甲酸(HCOOH)与甲醇(CH3OH)酯化反应的实验,回答以下问题:
某化学兴趣小组用甲、乙两套装置(如图所示)进行甲酸(HCOOH)与甲醇(CH3OH)酯化反应的实验,回答以下问题:查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二上学期期中考试化学试卷(选修)(解析版) 题型:选择题
甲酸(HCOOH)的下列性质中,可以证明它是弱电解质的是
A.甲酸溶液中有大量的HCOOH分子和H+、HCOO—
B.甲酸能与水以任意比例互溶
C.10mL 1 mol/L甲酸恰好与10mL 1 mol/LNaOH溶液完全反应
D.在相同温度下,相同浓度的甲酸溶液的导电性比盐酸弱
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com