
(1)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体类型为 。
(2)①CH2=CH2、②CH≡CH、③  、④CH3—CH3这四种分子中碳原子采取sp2杂化的是 (填序号)。
、④CH3—CH3这四种分子中碳原子采取sp2杂化的是 (填序号)。

(3)如图为某晶体的一个晶胞示意图,该晶体由A、B、C三种基本粒子组成,则该晶体的化学式为 。
科目:高中化学 来源:2016-2017学年天津市部分区高一上学期期末化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
B.铁粉溶于浓盐酸:Fe+2H+=Fe2++H2↑
C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
D.小苏打溶液中加入盐酸:CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:实验题
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中 是氧化剂,该反应中氧化产物与还原产物的物质量之比为 。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是: 。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液 mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式并用双线桥法表示出电子转移情况: 。
(5)现需490 mL 2.0 mol·L-1NaOH溶液:
①所需称量的氢氧化钠固体的质量是 。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、 。
③在配制溶液的过程中,下列操作可能造成结果偏高的是 。
A.定容时俯视 |
B.容量瓶不干燥,含有少量蒸馏水 |
C.溶解所用烧杯未洗涤 |
D.NaOH溶解后,未冷却即进行实验 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:选择题
将标准状况下的V L HCl(气)溶于1000 g水中,得到的盐酸密度为ρ g·cm-3,则该盐酸的物质的量浓度为
A.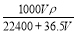 mol·L-1 B.
mol·L-1 B.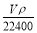 mol·L-1
mol·L-1
C. mol·L-1 D.
mol·L-1 D.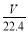 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高二上学期期末化学试卷(解析版) 题型:填空题
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下表。
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 地壳中含量最多的元素 |
Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
R | 核电荷数是Y与Q的核电荷数之和 |
E | N能层上只有一个电子,K、L、M层均排满电子 |
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图: 。X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为 。
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号) 。
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式) ,原因是 。
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式: 。
(5)R的一种配合物的化学式为RCl3·6H2O。已知0.01 mol RCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为: ,继续滴加氨水至过量,沉淀溶解,得到天蓝色溶液,写反应的离子方程式为: 。
(7)元素E的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
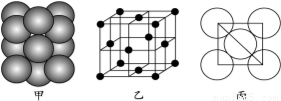
若已知该元素的原子半径为d cm,相对原子质量为M,NA代表阿伏加德罗常数,则该晶体的密度为 g·cm-3(用字母表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高二上学期期末化学试卷(解析版) 题型:选择题
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示该反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示该反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质B的浓度为0.7 mol·L-1
④2 s末,物质A的转化率为70%
其中正确的是
A.①④ B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高二上学期期末化学试卷(解析版) 题型:选择题
下列分子中,中心原子的杂化轨道类型相同,空间构型也相同的是
A.BeCl2 CO2 B.H2O SO2 C.BF3 NCl3 D.SiCl4 SO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高一上学期期末化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( S-32 O-16 )
A.标准状况下,22.4L氦气含有2NA个氦原子
B.在常温常压下,11.2L Cl2含有的分子数为0.5NA
C.常温常压下,64g SO2中含有的氧原子数为2NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高一上学期期末化学试卷(解析版) 题型:选择题
许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A .氯、溴、碘 B .钠、镁、铝 C.烧碱、氢气 D.食盐、淡水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com