(2013?江苏三模)某研究小组利用工业生产钛白粉产生的废液(含有大量的Fe
2+、H
+、S和少量的Fe
3+、TiO
2+)生产乳酸亚铁,其工艺流程如图所示:
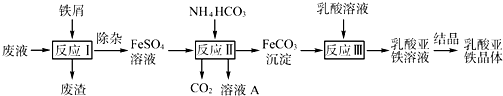
(1)反应Ⅰ中,铁屑与TiO
2+反应的离子方程式为2TiO
2++Fe+4H
+?2Ti
3++Fe
2++2H
2O,该反应的平衡常数表达式为K=
| c(Ti3+)2?c(Fe2+)2 |
| c(TiO2+)2?c(H+)4 |
| c(Ti3+)2?c(Fe2+)2 |
| c(TiO2+)2?c(H+)4 |
.
(2)反应Ⅱ需控制反应温度低于35℃,其目的是
防止NH4HCO3分解(或减少Fe2+的水解)
防止NH4HCO3分解(或减少Fe2+的水解)
,该反应的化学方程式是
FeSO4+2NH4HCO3═FeCO3↓+H2O+CO2↑+(NH4)2SO4
FeSO4+2NH4HCO3═FeCO3↓+H2O+CO2↑+(NH4)2SO4
.检验溶液A中是否含Fe
2+的实验操作方法是
取少量溶液A于试管中,滴入KSCN溶液,无明显现象,再滴入氯水,溶液呈血红色,证明有Fe2+;反之,不含有Fe2+
取少量溶液A于试管中,滴入KSCN溶液,无明显现象,再滴入氯水,溶液呈血红色,证明有Fe2+;反之,不含有Fe2+
.
(3)已知:FeCO
3(s)?Fe
2+(aq)+C(aq),试用平衡移动原理解释反应Ⅲ中生成乳酸亚铁的原因:
C与乳酸反应,其浓度降低,使平衡向右移动,碳酸亚铁溶解得到乳酸亚铁
C与乳酸反应,其浓度降低,使平衡向右移动,碳酸亚铁溶解得到乳酸亚铁
.
(4)结晶过程必须控制在一定的真空度条件下进行,原因是:
有利于水的蒸发
有利于水的蒸发
、
防止Fe2+被氧化
防止Fe2+被氧化
.




 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案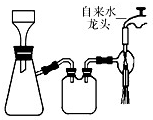 (2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下:
(2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下: