
| A.原子半径:Na>Mg>O |
| B.13C和14C属于同位素 |
| C.0族元素是同周期中非金属性最强的元素 |
| D.N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||
| 2 | | | | ① | ② | | ③ | | ||
| 3 | | ④ | ⑤ | | | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.R位于元素周期表中的第VA族 | B.R的氢化物的水溶液呈酸性 |
| C.RO3—中的R元素只能被还原 | D.R2在常温常压下一定是气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
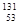 I,关于
I,关于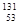 I的下列说法中正确的是( )
I的下列说法中正确的是( )A.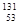 I是放射性核素,应该多吃加碘食盐来预防其对人体的损害 I是放射性核素,应该多吃加碘食盐来预防其对人体的损害 |
B.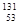 I与 I与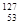 I属于碘元素的两种不同核素,互称同素异形体 I属于碘元素的两种不同核素,互称同素异形体 |
C.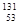 I与 I与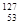 I属于同种元素,所以性质完全相同 I属于同种元素,所以性质完全相同 |
D.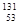 I核内中子数比核外电子数多25个 I核内中子数比核外电子数多25个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.m-13=n | B.m -5=n | C.m- n=8 | D.n-11=m |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔沸点:F2<Cl2<Br2<I2 | B.颜色:F2、Cl2、Br2、I2逐渐加深 |
| C.还原性: F―>Cl―>Br―>I― | D.热稳定性:HF>HCl>HBr>HI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com