
| �������� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 2 | A | B | C | |||||
| 3 | D | E | F | G | H | |||
| 4 | I |
 NH4++OH-
NH4++OH- NH4++OH-
NH4++OH- NH4++OH-��
NH4++OH-��

 ������ϵ�д�
������ϵ�д� �żӾ���ϵ�д�
�żӾ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
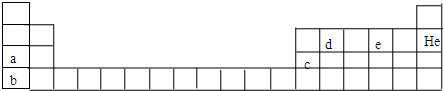
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | -1 | -2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ң�Ԫ�����ڱ��еĵ�ʮ����ΪVA�� | B��ijIIA��Ԫ�ص�ԭ������Ϊx��������ͬ���ڵ�IIIA��Ԫ�ص�ԭ����������Ϊx+25 | C��VIA��Ԫ�أ���ԭ�Ӱ뾶����Ӧ��̬�⻯����ȶ�����ǿ | D��53��Ԫ��λ�����ڱ��е�5����VIIA�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com