
����Ŀ��ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ��������ϵ��ʵ�顣
I.(1)���ơ��ء�þ������lmol �ֱ�Ͷ��������0.1 mol/L�������У���Ԥ��ʵ����:______�����ᷴӦ����ң�__________�����ᷴӦ������
(2)��NaOH��Һ��NH4CI��Һ�������NH3��H2O���Ӷ���֤NaOH�ļ��Դ���NH3��H2O���̶�������֤Na�Ľ����Դ���N�ģ�����Ϊ������Ƿ����?__________________���� ˵������__________________
II.������ͼװ�ÿ�����֤�ǽ����Եı仯���ɡ�

(3)�����D��������____________________________________________
(4)ʵ����������ҩƷNa2S��Һ��KMnO4��Ũ���ᡢMnO2�� ��ѡ�����ҩƷ���ʵ����֤�ȵķǽ����Դ������:װ��A. B��C����װҩƷ�ֱ�Ϊ________ ��_____________ ��________________, װ��C�е�ʵ������Ϊ�л�ɫ�������ɣ����ӷ���ʽΪ_____________________________________
(5)��Ҫ֤���ǽ�����: S>C>Si, ��A�м�__________��B�м�Na2CO3. C�м�________________���۲쵽C����Һ������Ϊ_________________________________
���𰸡��� �� ������ NΪ���÷ǽ����������ֳ������� ��ֹ���� Ũ���� KMnO4 Na2S S2- +Cl2=S��+2Cl- ϡ���� Na2SiO3��Һ �а�ɫ��������
��������
��ʵ��II�ķ�Ӧװ�ÿ��Կ�����A�Ƿ�Һ©����A�е�Һ�����������B�еĹ��巴Ӧ�������������ɣ���ͨ�����ܽ���C�У���C�е�Һ�巢����Ӧ��
(1)���ݽ����˳��K��Na��Mg��Al�Ľ��������μ�����������Խǿ�����ᷴӦԽ���ң����Լ������ᷴӦ��죬Al���ᷴӦ������
(2)һ������������Ԫ��֮��ȽϽ����ԣ��ǽ���Ԫ��֮��ȽϷǽ����ԣ�NԪ���Ƿǽ����������ֽ����ԣ����Է�����������
(3)��������ˮʱ��������Һ�嵹�������Ը����D�������Ƿ�ֹ������
(4)����û�м���װ�ã�ֻ���ø�������Ʊ�����������װ��B�еĻ�ѧ����ʽΪ
2KMnO4 + 16HCl= 2KCl + 2MnCl2 + 5Cl2��+ 8H2O�������ܰ���������Ϊ����S������װ��C�е�ʵ������Ϊ����dz��ɫ���������ӷ���ʽΪS2-+Cl2=S��+2C1-��
��5����Ҫ֤���ǽ����ԣ�C> Si�����������������ˮ���������ǿ�����Ƚϣ�����A�м����ᣬB�м�Na2CO3��C�м�Na2SiO3��CO2������Ʒ�Ӧ�������Na2SiO3 + CO2 + H2O = Na2CO3 + H2SiO3����H2SiO3�ǰ�ɫ�Ҳ�����ˮ�����Թ۲쵽C����Һ������Ϊ�а�ɫ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���Ԫ�������ɣ��ж�������������ȷ����
A. ��̬�⻯����ȶ��ԣ�H2O��NH3��SiH4
B. ��Ԫ��������Ԫ�ؿ��γɹ��ۻ���������ӻ�����
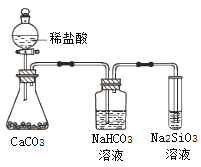
C. ��ͼ��ʾʵ���֤��Ԫ�صķǽ����ԣ�Cl��C��Si
D. ��������![]() ������o�������ĵ�118��Ԫ�������ڱ���λ�ڵ�������0��
������o�������ĵ�118��Ԫ�������ڱ���λ�ڵ�������0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���������AgCl�ֱ�������������У�AgCl���ܽ���ɴ�С������˳����(����)
��20 mL 0.01 mol��L��1KCl��Һ ��30 mL 0.02 mol��L��1CaCl2��Һ ��40 mL 0.03 mol��L��1HCl��Һ ��10 mL����ˮ ��50 mL 0.05 mol��L��1AgNO3��Һ
A. �٣��ڣ��ۣ��ܣ��� B. �ܣ��٣��ۣ��ڣ���
C. �ݣ��ܣ��ڣ��٣��� D. �ܣ��ۣ��ݣ��ڣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��һ�绯ѧʵ��װ��,ͼ��C��D��Ϊ���缫��UΪ���ţ�G�����������ƣ���ָ������ƫ���Դ������
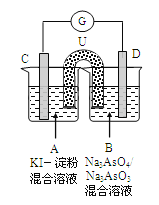
(1)As(��)λ��Ԫ�����ڱ��е�4���ڵڢ�A�壬��Na3AsO4��Һ��pH_________(�>����<����=��)7��
(2)��B���м���������Ũ�����ᣬ����G��ָ������ƫ�ơ���ʱA���е���Ҫʵ��������_____��D�缫�ϵĵ缫��ӦʽΪ___________��
(3)һ��ʱ�������B���м�����������������Ϊ40%������������Һ������G��ָ������ƫ�ơ���ʱ����ʵ��װ�õ��ܵ����ӷ���ʽΪ________________��
(4)�ٹ�һ��ʱ���G��ָ�����㣬��ʱʵ��װ���еĻ�ѧ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬���÷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪ��K=________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�����˵���������
A. PM2.5��ָ����������2.5��m�Ŀ���������������
B. ��ɫ��ѧҪ���Դͷ�����������������Ի�������Ⱦ
C. ȼú�м���CaO���Լ���������γɼ�����������ŷ�
D. ��Ȼ����Һ��ʯ�������ҹ�Ŀǰ�ƹ�ʹ�õ����ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ����
A. 2��3��3-�������� B. 2-������
C. ![]() 2-����ϩ D. 2��2-��������
2-����ϩ D. 2��2-��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������,��ӦaX(g)![]() bY(g)+cZ(g)�ﵽƽ��״̬,�����������䣬���������ѹ����ԭ����1/2,�Ҵﵽ�µ�ƽ��״̬ʱ,X�����ʵ���Ũ�ȴ�0.1 mol/L����0.19 mol/L,�����ж���ȷ����
bY(g)+cZ(g)�ﵽƽ��״̬,�����������䣬���������ѹ����ԭ����1/2,�Ҵﵽ�µ�ƽ��״̬ʱ,X�����ʵ���Ũ�ȴ�0.1 mol/L����0.19 mol/L,�����ж���ȷ����
A. a=b+c B. a=b=c C. a>b+c D. a<b+c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߷��ӻ�����G��һ�־������ϣ���һ�ֺϳ�·�����£�
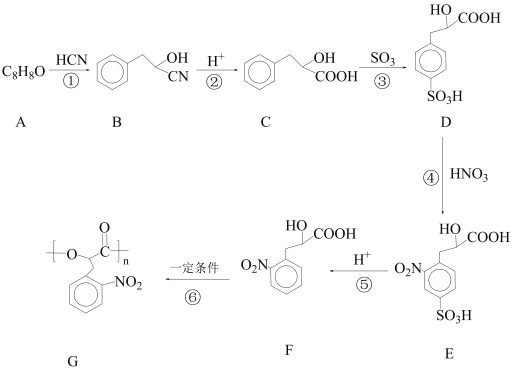
�ش��������⣺
(1)A��������________��B���еĹ�����������________��
(2)��Ӧ�ܵķ�Ӧ������________��
(3)��Ӧ�Ļ�ѧ����ʽΪ________��
(4)��Ӧ����������-SO3H��������________��
(5)��������������C��ͬ���칹�干��________�֣����������칹����
����ʹFeCl3��Һ����ɫ���ܷ���ˮ�ⷴӦ���ڱ�����������ȡ������
���к˴Ź���������ʾΪ5��壬�����֮��Ϊ3:2:2:2:1���Һ���-CH2CH3�����л���Ľṹ��ʽ��________ (��дһ�֣���
(6)��CH3CH2CH2OHΪԭ�ϣ�����Ʊ� �ĺϳ�·�ߣ�________��
�ĺϳ�·�ߣ�________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2O5��һ����������������һ���¶��¿ɷ������·�Ӧ��2N2O5(g)![]() 4NO2(g)��O2(g)����H ��0��T1�¶�ʱ�����ܱ�������ͨ��N2O5���壬����ʵ�����ݼ��±�������˵����ȷ����
4NO2(g)��O2(g)����H ��0��T1�¶�ʱ�����ܱ�������ͨ��N2O5���壬����ʵ�����ݼ��±�������˵����ȷ����
ʱ��/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/mol��L��1 | 5.00 | 3.50 | 2.50 | 2.50 |
A. 500 s��NO2����������Ϊ3.00��10��3 mol��L��1��s��1
B. T1�¶��¸÷�Ӧƽ��ʱN2O5��ת����Ϊ50%
C. ��ƽ��������������䣬���������ѹ����ԭ����![]() ��c(N2O5)<5.00 mol��L��1
��c(N2O5)<5.00 mol��L��1
D. T1�¶��µ�ƽ�ⳣ��ΪK1��T2�¶��µ�ƽ�ⳣ��ΪK2����T1>T2����K1<K2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com