
【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法正确的是
4NO2(g)+O2(g) ΔH >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法正确的是
时间/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/mol·L-1 | 5.00 | 3.50 | 2.50 | 2.50 |
A. 500 s内NO2的生成速率为3.00×10-3 mol·L-1·s-1
B. T1温度下该反应平衡时N2O5的转化率为50%
C. 达平衡后其他条件不变,将容器体积压缩到原来的![]() ,c(N2O5)<5.00 mol·L-1
,c(N2O5)<5.00 mol·L-1
D. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
【答案】B
【解析】
A. 500 s内N2O5分解速率为![]() =3.00×10-3 mol·L-1·s-1,因同一反应中,各物质表示的化学反应速率之比等于参加反应的化学计量数之比,则NO2的生成速率=
=3.00×10-3 mol·L-1·s-1,因同一反应中,各物质表示的化学反应速率之比等于参加反应的化学计量数之比,则NO2的生成速率=![]() =6.00×10-3 mol·L-1·s-1,A项错误;
=6.00×10-3 mol·L-1·s-1,A项错误;
B. 根据表格数据可知,反应达到平衡N2O5的物质的量浓度为2.50mol/L,故其转化率为![]() =50%,B项正确;
=50%,B项正确;
C. 体积压缩到原来的1/2,假设平衡不移动,N2O5的浓度为5mol·L-1,压强增大,平衡向逆反应方向移动,N2O5浓度增大,即大于5mol·L-1,C项错误;
D. 此反应是吸热反应,降低温度,平衡向逆反应方向移动,即K1>K2,D项错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计如下系列实验。
I.(1)将钠、钾、镁、铝各lmol 分别投入足量的0.1 mol/L的盐酸中,试预测实验结果:______与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4CI溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N的,你认为此设计是否合理?__________________。并 说明理由__________________
II.利用如图装置可以验证非金属性的变化规律。

(3)干燥管D的作用是____________________________________________
(4)实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2。 请选择合适药品设计实验验证氯的非金属性大于硫的:装置A. B、C中所装药品分别为________ 、_____________ 、________________, 装置C中的实验现象为有黄色沉淀生成,离子方程式为_____________________________________
(5)若要证明非金属性: S>C>Si, 则A中加__________、B中加Na2CO3. C中加________________,观察到C中溶液的现象为_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
(1)用三支试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴入0.1 mol·L-1 H2C2O4溶液,实验报告如下。

①实验1、3研究的是_________对反应速率的影响。
②表中V=_________mL。
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为KMnO4与H2C2O4的反应放热,温度升高,速率加快。
②乙同学认为随着反应的进行,因_________,故速率加快。
(3)为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:
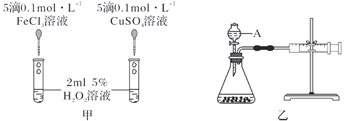
①装置乙中仪器A的名称为_________。
②定性如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是____________________________________。
③定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水的处理流程如图所示。

(1)①流程图设备Ⅰ中进行的是操作________(填写操作名称)。实验室里这一步操作可以用_______(填仪器名称)进行。
②由设备Ⅱ进入设备Ⅲ的物质A是______________(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是___________。
③在设备Ⅲ中发生反应的化学方程式为_____________________。
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和______。通过 _________________(填操作名称)操作,可以使产物相互分离。
⑤图中,能循环使用的物质是_______、_____________C6H6和CaO。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是____________。
从废水中回收苯酚的方法是①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③加入某物质又析出苯酚。试写出②、③两步的反应方程式:_________________________。
(3)为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,求此废水中苯酚的含量____________(mg·L-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下:Ksp(AgCl)=1.6×10-10,下列叙述正确的是 ( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的小
B.AgCl的悬浊液中c(Cl-)=4×10-5.5mol/L
C.将0.001 mol·L-1AgNO3溶液滴入0.001 mol·L-1的KCl,无沉淀析出
D.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法” 又叫“联合制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱Na2CO3,有关反应的化学方程式:
(1)______________。
(2)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是重要的有机物,可由E和F在一定条件下合成:(部分反应物或产物省略,另请注意箭头的指向)
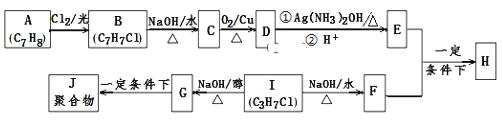
已知以下信息:
i.A属于芳香烃,H属于酯类化合物。
ii.I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)E的含氧官能团名称是 ______ ,B的结构简式是___________________。
(2)B→C和G→J两步的反应类型分别为 ___________,____________。
(3)①E+F→H的化学方程式是____________________________________。
②D与银氨溶液反应的化学方程式是__________________________________。
(4)E的同系物K比E相对分子质量大28,则K的同分异构体共 ______ 种,其中核磁共振氢谱显示为4组峰,且峰面积之比为6:2:1:1,写出符合要求的该同分异构体的结构简式为(写出1种即可) ____________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白钠镁矾(mNa2SO4·nMgSO4·xH2O)俗称硝板,工业上用白钠镁矾制备碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]晶须的过程如下:向碳酸钠溶液中加入白钠镁矾,保持50℃加热0.5h,有大量的5MgCO3·3H2O生成,然后升高温度到85℃加热2h发生热解反应,过滤得碱式碳酸镁晶体。
(1)热解反应的方程式为________________。
(2)碱式碳酸镁可用作化学冷却剂,原因是________________。
(3)为测定白钠镁矾的组成,进行下列实验:
①取白钠镁矾3.340 g溶于水配成100.00 mL溶液A;
②取25.00 mL溶液A,加入足量的氯化钡溶液,得BaSO4 1.165 g;
③另取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+(离子方程式为Mg2+ + H2Y2-=MgY2-+ 2H+),滴定至终点,消耗标准溶液25.00 mL。通过计算确定白钠镁矾的化学式(写出计算过程)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为_________________,其最外层电子的电子云形状为___________。
(2)(NH4)2Fe(SO4)26H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为_____________(用元素符号表示)。
②N、O两元素的的第一电离能由大到小的顺序为___________(用元素符号表示)。
③SO42-中S原子的杂化方式为___________,VSEPR模型名称为___________________。
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为_____,σ键和π键的数目之比为______________。其空间构型为__________。
(4)K3[Fe(CN)6]晶体中配离子的配位体为_____(用化学符号表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com