
【题目】金属氮化物具有高熔点、高硬度、高化学稳定性以及良好的导热、导电性,目前已经广泛应用于磁学、电子工业 、耐高温结构陶瓷等领域 。回答下列问题
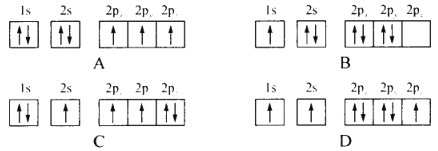
(1)下列不同状态的氮原子其能量最高的是________(填字母),基态氮原子处于最高能级的电子其电子云轮廓图形状为________
(2)第一电离能I1(N)______(填“> ”“< ”或“=”)I1(P),其原因是_____________。
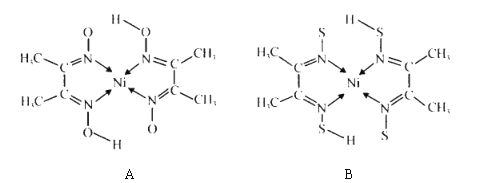
(3)A和B两种金属的含氮化合物的结构如图所示:
①基态 Ni 原子的核外电子排布式为[ Ar]________________。
②物质A 中碳原子的杂化方式为__________________。
③A的熔点高于 B 的,具主要原因是_______。
④B中含有的化学键类型有_____________(填字母)。
a.金属键 b. σ建
c.π键 d. 配位键
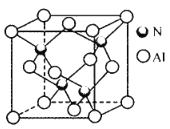
(4)氮化铝晶胞如图所示。氮原子的配位数为_______,每个铝原子周围紧邻__________个铝原子;已知立方氮化铝晶体密度为ρg cm-3,晶胞中最近的两个铝原子之间的距离为___pm(列出计算式即可,阿伏加德罗常数为6. 02×1023mol -1)。
【答案】D 哑铃形 > N的原子半径比P的小,原子核对最外层电子的吸引力较大 3d84s2 sp3、sp2 物质A分子间存在氢键 bcd 4 12 ![]() ×
×![]() ×1010
×1010
【解析】
(1)基态氮原子的核外电子排布式为1s22s2 2p3,离核越远的电子能量越高,处于2p能级的电子量最高;
(2)N和P位于同主族,半径越小,原子核对最外层电子的吸引力较大,则第一电离能更大;
(3)①基态Ni原子的核外电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;
②物质A 中碳原子有两种一种为甲基上的碳,类似于甲烷的四面体结构,另一种为C=N上的碳原子,结合碳原子的空间构型分析判断杂化类型;
③物质A、B结构相似,晶体类型相同,A中含有氢键,据此分析解答;
④根据B的结构图,B中含有配位键和共价键,配位键和共价单键都为σ键,双键中含有一个σ键和一个π键;
(4)由氮化铝晶胞图示中原子间位置关系判断配位数,该晶胞中Al原子位于晶胞的顶点和面心,则晶胞中Al原子的数目为8×![]() +6×
+6×![]() =4,N原子位于晶胞的内部,则N原子的数目为4,则晶胞的质量为
=4,N原子位于晶胞的内部,则N原子的数目为4,则晶胞的质量为![]() g,根据m=ρV计算晶胞的边长,晶胞中最近的两个铝原子之间的距离为晶胞面对角线长度的一半,据此计算解答。
g,根据m=ρV计算晶胞的边长,晶胞中最近的两个铝原子之间的距离为晶胞面对角线长度的一半,据此计算解答。
(1)氮原子其能量最高的是D,基态氮原子的核外电子排布式为1s22s2 2p3,离核越远的电子能量越高,处于2p能级的电子量最高,其电子云轮廓图形状为哑铃形;
(2)N和P位于同主族,N的原子半径比P的小,原子核对最外层电子的吸引力较大,则第一电离能I1(N)>I1(P);
(3)①基态Ni原子的核外电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;
②物质A 中碳原子有两种一种为甲基上的碳,类似于甲烷的四面体结构,该碳原子为sp3杂化,另一种为C=N上的碳原子,C=N是平面结构,则该碳原子为sp2杂化;
③物质A中的氧原子可形成分子间存在氢键,B中不能形成氢键,则A的熔点高于 B;
④根据B的结构图,B中含有配位键和共价键,配位键和共价单键都为σ键,双键中含有一个σ键和一个π键,只有金属晶体中含有金属键,则B中含有的化学键类型有σ键、π键、配位键,答案选bcd;
(4)由氮化铝晶胞图示可知,氮原子的配位数为4,每个铝原子周围紧邻12个铝原子;该晶胞中Al原子位于晶胞的顶点和面心,则晶胞中Al原子的数目为8×![]() +6×
+6×![]() =4,N原子位于晶胞的内部,则N原子的数目为4,则晶胞的质量为
=4,N原子位于晶胞的内部,则N原子的数目为4,则晶胞的质量为![]() g,根据m=ρV可得,晶胞的边长=
g,根据m=ρV可得,晶胞的边长=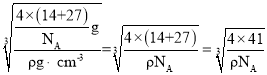 cm,晶胞中面对角线的长度为
cm,晶胞中面对角线的长度为![]() ×
×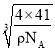 cm,晶胞中最近的两个铝原子之间的距离为晶胞面对角线长度的一半,则晶胞中最近的两个铝原子之间的距离为
cm,晶胞中最近的两个铝原子之间的距离为晶胞面对角线长度的一半,则晶胞中最近的两个铝原子之间的距离为![]() ×
×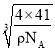 cm=
cm=![]() ×
×![]() ×1010 pm。
×1010 pm。


科目:高中化学 来源: 题型:
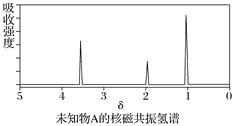
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的有( )
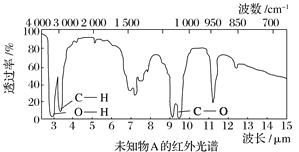
A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
D. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(HOOC-COOH)是一种常见的有机酸,利用淀粉制备草酸的实验流程如图:
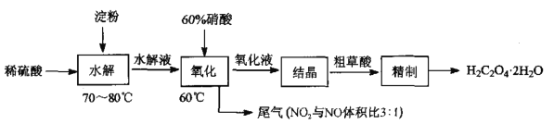
回答下列问题:
(1)“水解”时,检验淀粉是否水解完全,所用的试剂是____;“水解”及“氧化”步骤中适宜的加热方式是________________。
(2)“氧化”时实验装置如图所示(夹持及加热装置已略):
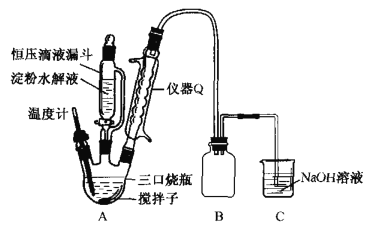
①仪器Q的名称是________.
②三口烧瓶中生成H2C2O4· 2H2O的化学方程式为____________。
③装置B的作用是___________,装置C的作用是_______________。
(3)已知在20℃、70℃时,草酸的溶解度依次为为9. 5 g/(l00g水),84.5g/(l00g水),则粗草酸“精制”需采用的提纯方法为___________________。
(4)探究H2C2O4的性质:
①向NaHCO3溶液中加入草酸溶液,产生大量气体,可得出草酸的酸性比碳酸_____(填“强”或“弱”)。
②向草酸中加入足量C2H5OH和适量浓硫酸加热,产生有芳香气味的油状物。该生成物为___________(写结构简式)。
③向K2Cr2O7溶液中加入H2C2 O4·2H2O析出K[Cr(C2O4)2(H2O)2]晶体,该反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A.0. 1 mol L-1的CaCl2 溶液中Ca2+的数目为0. lNA
B.标准状况 下,11. 2 L CHCl3 所含的分子数目为0. 5 NA
C.2. 8 g 乙烯含有的共用电子对的数目为 0. 6 NA
D.常温下,1 molFe与足量浓H2SO4反应,转移电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法制备磷酸二氢钾(KH2PO4)装置如图所示。下列说法正确的是
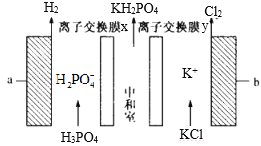
A.与 a 相连接的电源电势比 b 的高
B.离子交换膜 x、y 分别为阳离 子、阴离子交换膜
C.电解时,理论上相同时间内通过交换膜的阴、阳离子数相等
D.当外电路中通过 1mol 电子时,会有ll.2L的Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“达菲”是瑞士罗氏公司研制的有效治疗人类禽流感的药物。达菲的主要合成原料是我国盛产的莽草酸。


下列说法不正确的是( )
A.莽草酸可溶于水
B.1 mol莽草酸最多可和4 molNaOH溶液反应
C.从结构上推测,达菲既可与盐酸反应又可与氢氧化钠溶液反应
D.从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A、B、C互为同分异构体,分子式为C5H8O2,有关的转化关系如下图所示,已知A的碳链无支链,且1molA能与4molAg[(NH3)2]OH完全反应;B为五元环酯。
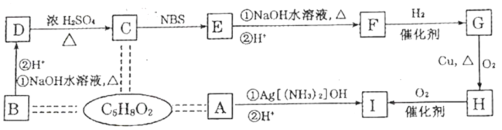
提示:CH3—CH=CH—R![]() Br—CH2—CH=CH—R
Br—CH2—CH=CH—R
(1)A中所含官能团是_____________。A与新制氢氧化铜悬浊液反应的方程式_________________________________。
(2)B、H的结构简式分别为_____________。
(3)写出下列反应方程式(有机化合物用结构简式表示)。
D→C:_____________________________________________________________。
E→F(只写①条件下的反应):_________________________________________。
(4)F的加聚产物的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法正确的是
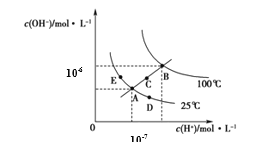
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到C点,可采用温度不变时在水中加入适量H2SO4 的方法
C.若从A点到D点,可采用在水中加入少量NaOH的方法
D.若处在B点温度时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推论正确的
A.![]() 的沸点高于
的沸点高于![]() ,可推测
,可推测![]() 的沸点高于
的沸点高于![]()
B.![]() 为正四面体结构,可推测出
为正四面体结构,可推测出![]() 也为正四面体结构
也为正四面体结构
C.![]() 晶体是分子晶体,可推测
晶体是分子晶体,可推测![]() 晶体也是分子晶体,
晶体也是分子晶体,
D.![]() 是碳链为直线型的非极性分子,可推测
是碳链为直线型的非极性分子,可推测![]() 也是碳链为直线型的非极性分子
也是碳链为直线型的非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com