
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O2 | |
| B. | 少量铜片放入浓硝酸中,有红棕色气体生成:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
分析 A.不加热条件下钠与空气中氧气反应生成氧化钠;
B.铜与浓硝酸反应生成硝酸铜、二氧化氮气体和水;
C.Na202在潮湿的空气中变成白色贴稠物的原因是过氧化钠与水反应生成了氢氧化钠和氧气;
D.氢氧化钙过量,反应生成碳酸钙沉淀、氢氧化钠和水.
解答 解:A.切开的金属Na暴露在空气中,光亮表面逐渐变暗,是由于钠与空气中氧气反应生成氧化钠,正确的反应为:4Na+O2═2Na2O,故A错误;
B.少量铜片放入浓硝酸中,有红棕色二氧化氮气体生成,反应的离子方程式为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故B正确;
C.Na202在潮湿的空气中先生成NaOH,则Na202在潮湿的空气中放置一段时间,变成白色贴稠物的原因是:2Na202+2H2O=4NaOH+O2↑,故C错误;
D.NaHCO3溶液中加入过量的澄清石灰水,反应生成碳酸钙沉淀、氢氧化钠和水,正确的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;试题培养了学生的灵活应用能力.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
 ,B在元素周期表的位置第二周期IVA族;
,B在元素周期表的位置第二周期IVA族; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 经测定某物质只含一种元素,则该物质一定是单质 | |
| B. | 阳离子、阴离子中均分别只含一种元素,则由这样的阴、阳离子组成的物质一定为纯净物 | |
| C. | 既能和酸反应又能和碱反应的化合物一定为两性化合物 | |
| D. | 酸性氧化物均可与强碱反应,碱性氧化物都是金属氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
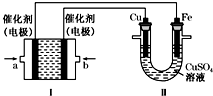 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸,消石灰,小苏打 | B. | 碳酸,乙醇,苛性钠 | ||
| C. | 硫酸,烧碱,水 | D. | 硫酸,纯碱,石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下甲烷和氧气的密度之比为2:1 | |
| B. | 1g甲烷和1g氧气的原子数之比为5:1 | |
| C. | 等物质的量的甲烷和氧气的质量之比为2:1 | |
| D. | 在标准状况下等质量的甲烷和氧气的体积之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、NaCl、SO2、NaCl溶液 | B. | BaSO4、SO3、CuSO4晶体、Na2O2 | ||
| C. | NaCl、H2S、CO2、Cu | D. | SO3、AgCl、NH3、H2O、Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$ 2Na+Cl2↑ | B. | MgO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | ||
| C. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$ 3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com