
【题目】下列图像正确的是( )
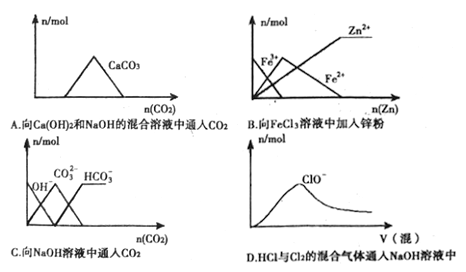
A. A B. B C. C D. D
【答案】B
【解析】A、Ca(OH)2和NaOH的混合溶液中通入CO2,二氧化碳先与氢氧根离子应产生碳酸根,生成碳酸钙沉淀,后与氢氧根离子反应无沉淀,最后碳酸钙与过量的二氧化碳反应使沉淀溶解,故A错误;B、向FeCl3溶液中加入锌粉,发生反应2Fe3++Zn=2Fe2++Zn2+,Zn+Fe2+=Fe+Zn2+,故三价铁一直减少,二价铁先增加后减少直至为0,锌离子慢慢增加最后不变,故B正确;C、向NaOH溶液中通入CO2,2OH-+CO2=CO32-+H2O,CO32-+CO2+H2O=2HCO3-,根据比例关系,氢氧根是碳酸根离子量的2倍,故C错误;D、HCl与Cl2的混合通入NaOH溶液中氢氧化钠先与盐酸反应,故开始不可能有次氯酸根离子产生,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定量混合气体发生下列反应: aM(g)+ bN(g)![]() cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是 ( )
cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是 ( )
A. 反应速率增大 B. 平衡向右移动 C. N的转化率提高 D. W的体积分数降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaHCO3和Na2O2的混合物放在密闭容器中加热,关于混合物加热前后与足量盐酸反应消耗盐酸的量,下列判断正确的是
A. 加热前后一样多
B. 加热前消耗的多
C. 加热后消耗的多
D. 当Na2O2适量时才会一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在短周期元素中,原子最外电子层只有1个或2个电子的元素是( )
A. 一定是金属元素 B. 可能是稀有气体元素 C. 一定不是非金属元素 D. 原子容易失去电子的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是( )
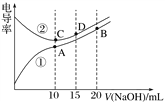
A. 曲线①代表滴定HCl溶液的曲线
B. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C三点溶液中水的电离程度:C<B<A
D. D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中通常伴随着能量变化,下列说法中错误的是
A.煤燃烧时将部分化学能转化为热能
B.电解熔融Al2O3时将部分化学能转化为电能
C.炸药爆炸时将部分化学能转化为动能
D.镁条燃烧时将部分化学能转化为光能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如下:
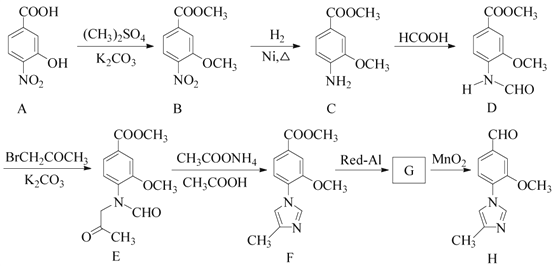
(1)C中的含氧官能团名称为_______和__________。
(2)D→E 的反应类型为__________________________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_____________________。 ①含有苯环,且分子中有一个手性碳原子;②能发生水解反应,水解产物之一是α-氨基酸,另一水解产物分子中只有2种不同化学环境的氢。
(4)G 的分子式为C12H14N2O2 ,经氧化得到H,写出G的结构简式:__________________。
(5)已知: ![]() (R代表烃基,R'代表烃基或H) 请写出以
(R代表烃基,R'代表烃基或H) 请写出以![]() 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) __________________。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。
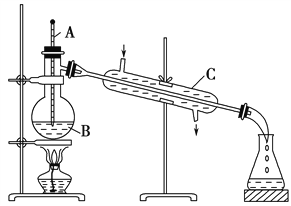
回答下列问题:
(1)指出图中的几处错误:____________________________。
(2)在除去工业酒精中的水时,下列做法不可取的是____________。
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰后分液
(3)由(2)可知除去工业酒精中的水的原理是(用化学方程式表示):_____________。
(4)装置中仪器A、B、C的名称分别是:A____________;B_______________;C_____________。
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
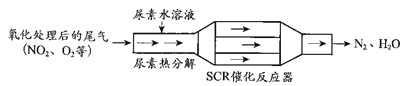
① 尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式:____________。
② 反应器中NH3还原CO2的化学方程式:____________。
③ 当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:________。
④ 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 mg·L1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是_________。
(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。
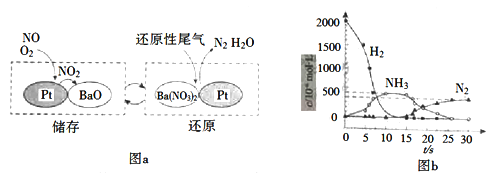
① 通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是_________。
② 用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__________。
③ 还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:_______![]() □15NNO+□H2O
□15NNO+□H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com