
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是
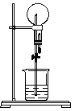
A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
科目:高中化学 来源: 题型:
【题目】手持技术的氧电化学传感器可用于测定 O2含量,右图为某种氧电化学传感器的 原理示意图。已知在测定O2含量过程 中,电解质溶液的质量保持不变。一定时 间内,若通过传感器的待测气体为aL(标 准状况),某电极增重了b g。下列说法正确的是

A.Pt电极为负极
B.反应过程中转移OH-的物质的量为0.125bmol
C.Pb电极上发生的电极反应为Pb-2e- +2OH- = Pb(OH)2
D.待测气体屮氧气的体积分数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物1,,3,5,7-辛四烯可用于制合成纤维、染料、药物等,其结构 简式为![]() 。该物质的合成方法如下图所示:
。该物质的合成方法如下图所示:
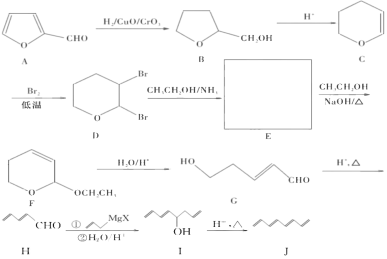
(1)1,3,5,7-辛四烯的分子式为______,有机物A所含含氧官能团有 _______(填名称)。
(2)E的结构简式为______.
(3)I→J的反应类型为______.
(4)![]() 在一定条件下可以发生加聚反应,合成无支链的链状有机高分子。写出该反应的化学方程式: ________________________ .
在一定条件下可以发生加聚反应,合成无支链的链状有机高分子。写出该反应的化学方程式: ________________________ .
(5)符合条件的G的同分异构体有___________种。
①与碳酸氢钠溶液反应产生气体 ②不能使溴水褪色
(6)以CH3CHO 、 HCHO和![]() 为原料也可以合成1,3,5,7-辛四烯,试写出合成路线。(其他试剂任选)_____________________________________________________________________ .已知:
为原料也可以合成1,3,5,7-辛四烯,试写出合成路线。(其他试剂任选)_____________________________________________________________________ .已知:![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.25℃,1 LpH=13的NaOH溶液中含有OH-的数目为0.1NA
B.标准状况下,4.6 g NO2和N2O4混合物中含氧原子数为0.3NA
C.标准状况下,6.72 L Cl2与水充分反应,转移电子数为0.3NA
D.0.1 mol/L NaHCO3溶液中,HCO3-、H2CO3和CO32-总数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 古人煮沸海水制取淡水,现代可通过向海水加入明矾实现海水淡化
B. 我国山水画所用的炭黑与“嫦娥四号”卫星所使用的碳纤维互为同分异构体
C. 某些筒装水使用的劣质塑料桶常含有乙二醇(![]() ),乙二醇不溶于水
),乙二醇不溶于水
D. “一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称,真丝绸的主要成分是蛋白质,属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a | |||||||||||||||||
b | c | d | e | ||||||||||||||
f | g | ||||||||||||||||
h | |||||||||||||||||
(1)请画出上述元素h的原子结构示意图_______;元素h位于元素周期表的第_____区。
(2)e、g两种元素的气态氢化物中更稳定的是_______(写化学式);
(3)b2a2分子的电子式是________ ,该分子中存在的σ键与π键的个数比为_______。
(4)c、d两种元素中第一电离能较大的是_________(写元素符号)。
(5)f和g两种元素形成的化合物是______(填“离子化合物”“共价化合物”)。a2d分子是_________分子(填极性分子或者非极性分子)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的恒容密闭容器中发生反应A(g)+2B(g)![]() 3C(g)。反应过程中的部分数据如下表所示:
3C(g)。反应过程中的部分数据如下表所示:
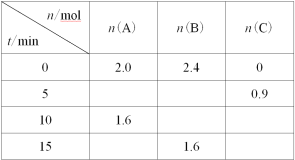
下列说法正确的是( )
A.0~5min用A表示的平均反应速率为0.09mol·L1·min1
B.该反应在10min后才达到平衡
C.平衡状态时,c(C)=0.6mol·L1
D.物质B的平衡转化率为20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。
2SO3(g)。
(1)降低温度,化学反应速率___(填“增大”“减小”或“不变”)。
(2)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,反应前15min用SO3表示的平均反应速率为___。
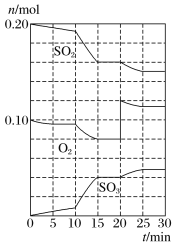
(3)已知0-15min反应放出的总热量为QkJ,写出该反应的热化学方程式____。
(4)根据如图判断,10min时改变的反应条件可能是___(填编号,下同);20min时改变的反应条件可能是____。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)(NH4)2SO4中含有化学键的类型为_________________________。
(2)KNO3中NO3-的立体构型为____________________,其中N原子的杂化方式为________,写出与NO![]() 互为等电子体的另一种阴离子的化学式:_______________。
互为等电子体的另一种阴离子的化学式:_______________。
(3)已知配合物CrCl3·6H2O中心原子Cr3+的配位数为6,向含0.1 mol CrCl3·6H2O的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50 mL,则该配合物的化学式为________________,Cr在基态时,价电子排布式为_____________________。
(4)LiBH4由Li+和BH4-构成,BH4-的立体构型是____________,根据化合物LiBH4判断,Li、B、H的电负性由大到小的顺序为____________。
(5)丙酮(![]() )分子中C原子轨道杂化类型为_____________;含有的π键与σ键数目之比为___________。
)分子中C原子轨道杂化类型为_____________;含有的π键与σ键数目之比为___________。
(6)第一电离能I 1(Zn)______I 1(Cu)(填“大于”或“小于”),原因是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com