
【题目】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a | |||||||||||||||||
b | c | d | e | ||||||||||||||
f | g | ||||||||||||||||
h | |||||||||||||||||
(1)请画出上述元素h的原子结构示意图_______;元素h位于元素周期表的第_____区。
(2)e、g两种元素的气态氢化物中更稳定的是_______(写化学式);
(3)b2a2分子的电子式是________ ,该分子中存在的σ键与π键的个数比为_______。
(4)c、d两种元素中第一电离能较大的是_________(写元素符号)。
(5)f和g两种元素形成的化合物是______(填“离子化合物”“共价化合物”)。a2d分子是_________分子(填极性分子或者非极性分子)。
【答案】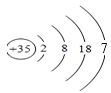 p HF
p HF ![]() 3:2 N 共价化合物 极性分子
3:2 N 共价化合物 极性分子
【解析】
由元素在周期表中位置,可知a为H、b为C、c为N、d为O、e为F、f为Al、g为Cl、h为Br。
(1)h为Br,原子核外有35个电子,有4个电子层,各层电子数为2、8、18、7;
(2)非金属性越强,氢化物越稳定;
(3)C2H2分子中C原子之间形成3对共用电子对,C原子与H原子之间形成1对共用电子对,其结构式为H-C≡C-H,单键为σ键、三键含有1个σ键、2个π键;
(4)同一周期的元素原子序数越大,第一电离能也越大,但第IIA、第VA元素处于全满、半满的稳定状态,第一电离能比相邻的元素大;
(5)Al、Cl形成的化合物是AlCl3,该物质是共价化合物,a2d分子是H2O,根据分子中原子的空间排列判断分子极性。
由元素在周期表中位置,可知a为H、b为C、c为N、d为O、e为F、f为Al、g为Cl、h为Br。
(1)h为Br,原子核外有35个电子,有4个电子层,各层电子数为2、8、18、7,原子结构示意图为 ;元素h位于元素周期表的第四周期第VIIA,属于p区;
;元素h位于元素周期表的第四周期第VIIA,属于p区;
(2)同主族自上而下非金属性减弱,非金属性F>Cl,元素的非金属性越强,其相应的简单氢化物越稳定,所以氢化物稳定性:HF>HCl,即HF更稳定;
(3) b2a2分子是C2H2,在该物质分子中C原子之间形成3对共用电子对,C原子与H原子之间形成1对共用电子对,电子式为:![]() ,结构式为H-C≡C-H,共价单键为σ键、共价三键含有1个σ键、2个π键,故σ键与π键的个数比为3:2;
,结构式为H-C≡C-H,共价单键为σ键、共价三键含有1个σ键、2个π键,故σ键与π键的个数比为3:2;
(4)N的电子排布式为1s22s22p3,2p轨道半充满,能量较低,较稳定,O的电子排布式为1s22s22p4,2p轨道易失去一个电子形成半充满的稳定状态,所以N元素第一电离能高于同周期相邻元素,即N、O两种元素中第一电离能较大的是N元素;
(5)Al、Cl形成的化合物是AlCl3,该物质是由分子构成的共价化合物,a2d分子是H2O,在水分子中两个H-O键之间的夹角是104.3°,分子空间排列不对称,因此该物质分子是极性分子。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化饰(CeO2)在太阳能作用下将H2O、CO2转变为H2、 CO,其过程如下所示:
mCeO2![]() (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+x H2O+xCO2![]() mCeO2+xH2+xCO2
mCeO2+xH2+xCO2
下列说法不正确的是
A.该过程中CeO2是H2O、CO2转变为H2、CO反应的催化剂
B.利用CeO2作催化剂-既可使该转变过程速率提高。亦可减小能量的消 耗,并可提高反应物转化率
C.mmol CeO2参加反应,气体物质的量增加x mol
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH - - 2e = CO32- +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向10 mL 0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是( )
A. 溶液中离子的数目减小
B. 再加入CH3COONa固体能促进醋酸的电离
C. 醋酸的电离程度增大,c(H+)亦增大
D. 溶液中c(CH3COO-)/c(CH3COOH)c(OH-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。回答下列问题:
(1)该混合气体的平均摩尔质量:_________________________。
(2)混合气体中碳原子的个数:_________________________
(用NA表示阿伏加德罗常数的值)。
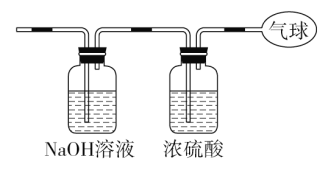
(3)将混合气体依次通过如图装置,最后收集在气球中。
①气球中收集到的气体摩尔质量:_______________________;
②标况下气球中收集到的气体的体积为___________________;
③气球中收集到的气体的电子总数为_____________________
(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是

A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.室温下浓度均为0.1 mol/L的盐酸和氨水混合呈中性时,消耗盐酸的体积大于氨水
B.室温下向0.1 mol/L氨水中加入等浓度等体积的盐酸,溶液导电能力增强
C.室温下pH相等的CH3COOH溶液和盐酸中,c(OH-)相等
D.室温下pH=1的CH3COOH溶液和pH=13的NaOH溶液中,c(CH3COO-)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行如下反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-764.5kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g) △H=-764.5kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度
B.升高温度同时充入氮气
C.加催化剂同时增大压强
D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原液流电池是一种新型绿色的二次电池。其工作原理如图所示。下列叙述正确的是

A.电子由Y极流出,经质子交换膜到X极
B.放电过程中,电解质溶液pH降低
C.Y极反应式为V2+-e-=V3+
D.每转移1 mol,电子理论上有2 mol H+由交换膜右侧向左侧迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①![]() ②(CH3)3CBr ③(CH3)3CCH2Cl ④CHCl2CHBr2 ⑤
②(CH3)3CBr ③(CH3)3CCH2Cl ④CHCl2CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A. ①③⑥B. ②③⑥C. 全部D. ①②⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com