
(16分)某研究性学习小组为研究铁粉与浓硫酸反应所生成气体的成份并测定各气体的含量,进行了如下实验:【实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体。
(1)该小组作出此推测的理由是: 。
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2 mol/L的H2C2O4标准溶液、0.1 mol/L的酸性KMnO4标准溶液、酸碱指示剂。
b.实验装置设计及组装(加热及夹持装置均已略去)

【实验过程及数据处理】
(2)B中发生反应的离子方程式为: 。
(3)实验前先通入一段时间的N2,其目的是 。
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
。
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25 mL,用H2C2O4标准溶液进行测定。
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平。
( )H2C2O4+( )MnO4- +( )H+ =( )Mn2+ +( ) H2O+( ) ( )
②反应完全的现象是 。
③重复测定两次,平均每次耗用H2C2O4标准溶液15.63 mL,则铁与浓硫酸反应产生的SO2气体
的物质的量为 ;经称量,实验前后装置D的质量减少0.8 g,则产生的气体中SO2的体积分数为 。
(16分) (1)在加热的条件下浓硫酸与Fe反应生成SO2,随着反应的进行,硫酸浓度变稀,与Fe反应生成H2
(2) 5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
(3) 排除装置中的空气,防止H2与空气混合受热发生爆炸。
(4) B瓶中溶液紫红色变浅说明生成了SO2,D中黑色粉末变红说明生成了H2。(答对一种得1分)
(5) ①5、2、6、2、8、10CO2
②滴入最后一滴H2C2O4溶液时KMnO4溶液的紫红色褪去且半分钟之内不恢复。
③0.025 mol, 33.3%
【解析】
试题分析:(1)在加热的条件下浓硫酸与Fe反应生成SO2,随着反应的进行,硫酸浓度变稀,与Fe反应生成H2,所以足量的铁与浓硫酸反应产生的气体可能是二者的混合气体;
(2)B中发生的反应是二氧化硫与酸性高锰酸钾溶液发生的氧化还原反应,离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
(3)实验中产生的氢气与空气混合易发生爆炸,所以实验前先通入一段时间的N2,目的是排除装置中的空气,防止H2与空气混合受热发生爆炸。
(4)二氧化硫与酸性高锰酸钾反应,使溶液颜色变浅或褪色,氢气还原氧化铜有Cu生成,使黑色固体变红,所以实验现象是B瓶中溶液紫红色变浅说明生成了SO2,D中黑色粉末变红说明生成了H2。
(5)①H2C2O4中的C元素是+3价,产物应升高到+4价,所以空白处的产物是CO2,升高2价,MnO4-中的Mn是+7价,产物中的Mn是+2价,降低5价,根据得失电子守恒,可知H2C2O4的系数是5,MnO4-,的系数是2,从而CO2的系数是10,Mn2+,的系数是2,再根据电荷守恒配平H+的系数是6,最后根据质量守恒配平H2O的系数是8;
②高锰酸钾溶液为紫色溶液,当反应完全时滴入最后一滴H2C2O4溶液,KMnO4溶液的紫色褪去且半分钟之内不恢复;
③实验中消耗H2C2O4的物质的量是0.2 mol/L×15.63×10-3L=3.126×10-3mol,则反应后B溶液中的高锰酸钾的物质的量是3.126×10-3mol×2/5×8=0.01mol,所以用于和二氧化硫反应的高锰酸钾的物质的量是0.1mol/L×0.2L-0.01mol=0.01mol,则B中吸收二氧化硫的物质的量是0.01mol×5/2=0.025mol;
根据D中的固体的质量的减少值,可计算氢气的物质的量。
CuO+H2=Cu+H2O, 固体质量减少
1mol 16g
n 0.8g
解得n=0.05mol,
所以混合气体中有0.025mol的SO2和0.05mol的H2,实验后二氧化硫的体积分数也是物质的量分数是0.025/(0.025+0.05) ×100%=33.3%.
考点:考查铁与浓硫酸的反应实验,气体的检验,氧化还原反应的计算,离子方程式的书写与配平,实验现象的判断,对实验的分析


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列物质分类正确的是
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是
A.植物通过光合作用将CO2转化成葡萄糖是太阳能转变成热能的过程
B.油脂属于酯类化合物,油脂的水解反应叫皂化反应
C.淀粉与纤维素互称为同分异构体
D.浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.常温下,0.1 mol·L—1Na2S溶液中存在:c(OH—)=c(H+) + c(HS—) + c(H2S)
B.常温下,0.1 mol·L—1HA溶液与0.1 mol·L—1 NaOH溶液正好完全反应时,溶液中一定存在:c(Na+)=c(A—)>c(OH—)=c(H+)
C.常温下,向0.1 mol·L—1CH3COOH 溶液加水稀释,当溶液的pH从3.0升到4.0时,
溶液中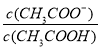 的值增大到原来的10倍
的值增大到原来的10倍
D.常温下,pH=7的CH3COONa和CH3COOH混合溶液中:
c(Na+)=c(CH3COOH)>c(CH3COO—)>c(H+)=c(OH—)
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列各项实验操作不能达到目的的是
A.在蔗糖溶液中加入几滴稀硫酸,水浴加热5 min,加入NaOH溶液至碱性,
再加入银氨溶液并水浴加热检验葡萄糖的生成
B.苯中混有苯酚可与足量氢氧化钠溶液反应后分液除去
C.使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素
D.只用溴水一种试剂即可鉴别甲苯、己烯、乙醇、四氯化碳四种液体
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:
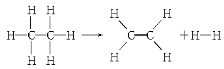
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是( )
A.该反应放出251.2 kJ的热量 B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量 D.该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由C经导线流向D;③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D相连后,同时浸入稀H2SO4溶液中,B极发生氧化反应。据此,判断四种金属的活动性顺序是( )
A.A>B>D>C B.A>C>D>B C.C>A>B>D D.B>D>C>A
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市高三六校第二次联考理综化学试卷(解析版) 题型:选择题
在阿司匹林的结构简式(如图)中①②③④⑤⑥分别标出了其分子不同的键。将阿司匹林与足量NaOH溶液共热时,发生反应时断键的位置是( )
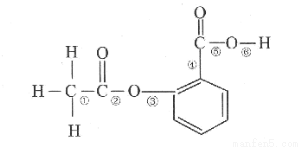
A.①④
B.②⑤
C.③④
D.②⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014江西八一中学、洪都中学下学期期中考试高一化学试卷(解析版) 题型:选择题
核电荷数小于l8的某元素X,其原子的电子层数为n,最外层电子数为(2n+1),原子核内质子数为(2n2-1)。下列关于元素X的说法中,不正确的是
A.其最高化合价为+3 B.可以形成化学式为KXO3的盐
C.其氢化物可以用来做喷泉实验 D.其最高价氧化物的水化物是强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com