
【题目】下列实验不能达到实验目的或者实验操作不正确的是 ( )
A. 定容 B. 比较硫、碳、硅三种元素的非金属性
B. 比较硫、碳、硅三种元素的非金属性 C. 尾气处理
C. 尾气处理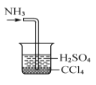 D. 测定黄铜中锌的含量
D. 测定黄铜中锌的含量
【答案】A
【解析】
A.容量瓶定容时,距离刻度线1-2cm时改用胶头滴,故A错误;B.若锥形瓶中生成气体,说明硫酸的酸性比碳酸强,烧杯中生成白色沉淀,说明碳酸的酸性比硅酸强,最高价氧化物对应水化物酸性越强,则对应元素的非金属性越强,因此比较硫、碳、硅非金属性强弱的实验方案合理,所以B正确的;C.氨气易溶于水和硫酸,难溶于四氯化碳,四氯化碳的密度比硫酸溶液大,导管口伸入下层液体可以防止倒吸,逸出的氨气被稀硫酸完全吸收生成铵盐,所以C是正确的;D.锌是氢前金属,铜是氢后金属,前者与稀盐酸发生置换反应,生成的氢气难溶于水,水还能除去氢气中混有的氯化氢,排水量气法收集氢气,根据氢气的体积可以计算完全反应的锌的质量,进而可以求黄铜中锌的含量,所以D是正确的;答案:A。


科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,把装有NO和NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的![]() ,则原混合气体中NO和NO2的体积比为( )
,则原混合气体中NO和NO2的体积比为( )
A. 3∶lB. 1∶3C. 2∶3D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100 ℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,Ⅰ容器0.1mol N2O4 Ⅱ容器0.2 mol NO2,发生反应:2NO2(g) ![]() N2O4(g) ΔH<0,下列说法正确的是( )
N2O4(g) ΔH<0,下列说法正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4) +α(NO2)=1
B. 平衡后,再向Ⅱ容器内通入一定量的NO2,又达到平衡时,NO2的体积分数增大
C. 若只改变一个条件使Ⅱ容器NO2的平衡转化率增大,则该反应的化学平衡常数一定变大
D. 平衡后,反应放出或吸收热量的数值Q:Q(Ⅰ) =Q(Ⅱ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
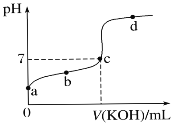
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中反应:A2+B2![]() 2AB,产物AB的生成情况如图所示,a为500℃,b为300℃ 时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是
2AB,产物AB的生成情况如图所示,a为500℃,b为300℃ 时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是

A. A2、B2、AB均为气体,正反应放热
B. AB为气体,A2、B2中最少有一种为非气体,正反应吸热
C. AB为气体,A2、B2中最少有一种为非气体,正反应放热
D. AB为固体,A2、B2中最少有一种为非气体,正反应吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g)△H>0;向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g)△H>0;向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |

A. 甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B. 丙容器的体积V>0.5L
C. 当温度为T1℃时,反应的平衡常数K=2.25
D. 乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下列知识,回答(1)、(2)问题。
Ⅰ.结构中没有环状的烷烃又名开链烷烃,其分子式是CnH2n+2(n为正整数),分子中每减少2个碳氢键,必然同时会增加1个碳碳键。它可能是重键(双键或叁键),也可能是连接环状烃。都称为增加了一个不饱和度(用希腊字母Ω表示。又称“缺氢指数”)。如丙烯的Ω=1;苯的Ω=4。
Ⅱ.在有机物分子中,当某个碳原子所连的是4个不同的原子或原子团,该碳原子叫不对称碳原子,通常用星号标出(*C),并具有特殊的光学活性。
(1)据报道,最近有人首次人工合成了一种有抗癌活性的化合物Depudecin这种物质曾从真菌里分离出来,其结构如图所示:

①试写出这种化合物的分子式________________;该化合物的Ω为____________。
②这个分子的结构里有__________个不对称碳原子?请在题目中给出的结构简示里用*把它们表示出来。
(2)新近合成的某有机物经测定具有光学活性,其结构式如图所示:

若要使该有机物不再具有光学活性,你可采用哪些化学方法?请分别列出:__________________、__________________、__________________(写出三种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一定体积的密闭容器中,下列叙述不能作为可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡状态标志的是 ( )
2C(g)达到平衡状态标志的是 ( )
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A. ②⑧B. ④⑦C. ①③D. ⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com