

分析 铝土矿可以看做Al2O3、MgO、Fe2O3、SiO2组成,铝土矿加过量盐酸溶解后,MgO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解,不溶物为SiO2,溶液A中含有镁离子、铁离子和铝离子、氢离子,加入过量烧碱,氢离子和氢氧化钠反应生成水,镁离子、铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化镁、氢氧化铁不溶于氢氧化钠溶液中,但氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,溶液D中通入过量CO2生成沉淀F,为偏铝酸根离子和二氧化碳能发生反应生成氢氧化铝沉淀,根据流程图沉淀F为氢氧化铝转化为物质M为氧化铝;
(1)过滤是用来分离不溶性固体和液体混合物的方法;
(2)铝土矿可以看做Al2O3、MgO、Fe2O3、SiO2组成,铝土矿加过量盐酸溶解后,MgO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解,不溶物为SiO2;沉淀C为加入烧碱后的沉淀,所以沉淀为氢氧化物,Fe(OH)3、Mg(OH)2,溶液D中大量存在的阴离子是AlO2-、Cl-、OH-;
(3)根据流程图沉淀F为氢氧化铝转化为物质M为氧化铝,据此书写方程式;沉淀B为SiO2可以写出与烧碱的反应方程式.
解答 解:(1)分离不溶于水的固体和液体,可用过滤的方法,故答案为:过滤;
(2)铝土矿加过量盐酸溶解,MgO、Fe2O3、Al2O3和HCl反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,
Al2O3+6HCl=2AlCl3+3H2O.而SiO2不与盐酸反应,所以沉淀B为不溶物SiO2;
滤液A中含有的阳离子有Fe3+、Al3+、Mg2+、H+,加入过量烧碱,氢离子和氢氧化钠反应生成水,镁离子、铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,所以沉淀C的成分是氢氧化镁、氢氧化铁;
氢氧化镁、氢氧化铁不溶于氢氧化钠溶液中,但氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,所以溶液D中大量存在的阴离子是AlO2-、Cl-、OH-其中AlO2-、Cl-是酸根离子,
故答案为:SiO2;Fe(OH)3、Mg(OH)2;AlO2-、Cl-;
(3)根据流程图沉淀F为氢氧化铝,氢氧化铝受热分解生成氧化铝和水,反应为:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,二氧化硅和氢氧化钠反应生成硅酸钠和水,离子反应为SiO2+2OH-=SiO32-+H2O,
故答案为:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;SiO2+2OH-=SiO32-+H2O.
点评 本题主要考查了元素化合物中金属铝、铁的性质,解题时不仅需熟知物质间的反应原理,还需灵活运用于实验的设计,题目难度不大.


科目:高中化学 来源: 题型:解答题
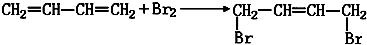

 ;C
;C .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用NH4Cl与NaNO2溶液混合微热制N2 | |
| B. | SnCl4与水的反应:SnCl4+2H2O═SnO2+4HCl | |
| C. | 人工树叶制取甲烷:CO2+2H2O$\frac{\underline{\;\;\;\;\;\;\;光\;\;\;\;\;\;\;}}{人工树叶}$CH4+2O2 | |
| D. | 银针验毒:4Ag+2H2S+O2═2Ag2S+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②中无色气体中有NO,可能含CO2 | |
| B. | ③中沉淀有BaSO4,可能含BaCO3 | |
| C. | 肯定存在的离子是Al3+、SO42-、NO3-、Mg2+,肯定不存在的离子是Ba2+、Fe2+、CO32-、I-,不能确定的离子是K+、Cl- | |
| D. | ②中红棕色气体通入水中发生反应的离子方程式为:3NO2+H2O═H++NO3-+2NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 应用李比希法、钠熔法、铜丝燃烧法、元素分析仪都可确定有机化合物的元素组成 | |
| B. | 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物组成元素和结构的分析 | |
| C. | 运用同位素示踪法可确定有机物的反应机理 | |
| D. | 可用酸性高锰酸钾溶液或溴水鉴定某有机物分子中是否含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 过氧化氢是重要的氧化剂和还原剂,常周于消毒、杀菌、漂白等.某化学兴趣小组同学.围绕着过氧化氢开展了调査研究与实验.
过氧化氢是重要的氧化剂和还原剂,常周于消毒、杀菌、漂白等.某化学兴趣小组同学.围绕着过氧化氢开展了调査研究与实验.| 实验编号 | T/X | H2O2初始浓度/moL•L-1 | FeCl3初始浓度/moL•L-1 |
| I | 20 | 1.0 | 0 |
| n | 50 | 1.0 | 0 |
| in | 50 | 1.0 | 0.1 |
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| n(M):n(H2O) | M转化率 | H2O转化率 |
| 1:1 | 0.5 | 0.5 |
| 1:2 | 0.67 | 0.33 |
| 1:3 | 0.75 | 0.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com