
分析 (1)依据C=$\frac{1000ρω}{M}$计算次氯酸钠物质的量浓度;
(2)依据溶液稀释过程中溶质的物质的量不变计算解答;
(3)根据溶液的配制及c=$\frac{n}{V}$、m=nM来分析;
(4))①根据c(H2SO4)=$\frac{1}{2}$c(H+)计算;
②根据溶液稀释前后溶质的物质的量不变计算.
解答 解:(1)质量分数37.25%,密度1.2g•cm-3的次氯酸钠物质的量浓度C=$\frac{1000×37.25%×1.2}{74.5}$=6.0mol/L;
故答案为:6.0;
(2)稀释前后溶液中NaClO的物质的量不变,则有:100 mL×10-3 L•mL-1×6.0 mol•L-1=100 mL×100×10-3 L•mL-1×c(NaClO),解得稀释后c(NaClO)=0.06 mol•L-1,c(Na+)=c(NaClO)=0.06 mol•L-1,
故答案为:0.06;
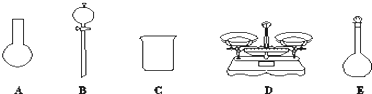
(3)A.需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的A、B、不需要,但还需玻璃棒和胶头滴管,故A错误;
B.配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用,故B错误;
C.由于NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少,配制的溶液中溶质的物质的量减小,结果偏低,故C正确;
D.应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以需要NaClO的质量:0.5 L×6.0 mol•L-1×74.5 g•mol-1=223.5 g,故D错误;
故答案为:C;
(4)①根据H2SO4的组成可知,溶液中c(H+)=2c(H2SO4),c(H2SO4)=2.3mol•L-1,则c(H+)=4.6mol•L-1,
故答案为:4.6;
②溶液稀释前后溶质的物质的量不变,浓硫酸的浓度为c=$\frac{1000×1.84×98%}{98}$=18.4mol/L,假设需要浓硫酸的体积为V,则V×18.4mol/L=1L×2.3mol/L,V=0.125L=125.0mL,
故答案为:125.0.
点评 本题考查物质的量浓度的计算以及溶液的配制,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X和Y的总能量一定高于M和N的总能量 | |
| B. | X能量一定高于Y | |
| C. | 因该反应为放热反应,故不必加热就可发生 | |
| D. | Y能量一定高于N |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下NaHCO3产生的CO2体积大 | |
| B. | 等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍 | |
| C. | 将石灰水加入NaHCO3溶液中无沉淀,加入Na2CO3溶液中有白色沉淀 | |
| D. | 等浓度的两种盐溶液分别与等浓度的盐酸反应,碳酸氢钠溶液的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池正极反应式为:2MnO2+2e-+2H2O═2MnOOH+2OH- | |
| B. | 该电池反应中MnO2起催化作用 | |
| C. | 该电池工作时电流由Zn经导线流向MnO2 | |
| D. | 该电池中Zn作负极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸乙酯 | B. | 乙酸甲酯 | C. | 乙酸丙酯 | D. | 丙酸丁酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com