
科目:高中化学 来源:2016-2017学年广东省揭阳市高二下学期第一次月考理科综合化学试卷(解析版) 题型:推断题
聚酯增塑剂广泛应用于耐油电缆、煤气管、防水卷材、电气胶带;耐油耐汽油的特殊制品等。聚酯增塑剂G及某医药中间体H的一种合成路线如下(部分反应条件略去):
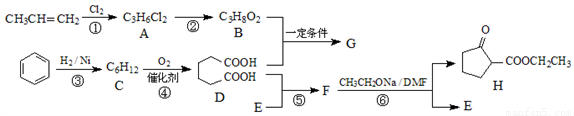
已知:
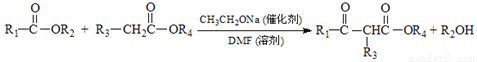
(1)B的名称(系统命名)为___________________。
(2)若反应①的反应条件为光照,最先得到的氯代有机物结构简式是_____________________。
(3)写出下列反应的反应类型:反应②是________________,反应④是________________ 。
(4)写出B与D反应生成G的反应方程式_________________________。
(5)甲苯的二氯代物产物的同分异构体有_________________种。
(6)利用以上合成路线的信息,以甲苯和乙醇为原料合成下面有机物(无机试剂任选)。
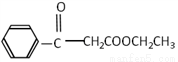
请写出合成路线:________________________________。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法错误的是
A. X、R的最高化合价相同
B. 简单离子的半径:X>Y>Z
C. Y、Z、R最高价氧化物对应水化物相互之间可以发生反应
D. 电解熔融的X与Z组成的化合物可以得到单质Z
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
根据能量变化示意图,下列说法正确的是
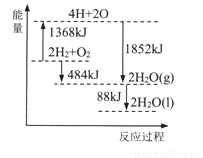
A. 拆开2molH2(g)和1 molO2(g)中的化学键,共放出1368 kJ能量
B. 1 molH2和0.5molO2的能量之和比1 molH2O(l)的能量大242 kJ
C. 2H2O(g)=2H2(g)+O2(g) △H=484kJ/mol
D. 2H2(g)+O2(g)=2H2O(l) △H=572kJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
X(g)+2Y(s)  2Z(g) △H=-akJ/mol,一定条件下,将1molX和2molY加入2L的恒容密闭容器中,10min后测得Y的物质的量为1.4mol。下列说法正确的是
2Z(g) △H=-akJ/mol,一定条件下,将1molX和2molY加入2L的恒容密闭容器中,10min后测得Y的物质的量为1.4mol。下列说法正确的是
A. 10min内,X的平均反应速率为0.03mol/(L·min)
B. 若容器中的气体密度不再发生变化,说明上述反应已达平衡状态
C. 10min后Z的浓度为0.7mol/L
D. 10min内,反应放出的热量为0.3kJ
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期开学考试化学试卷(解析版) 题型:简答题
湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。一种由铜镉渣生产金属镉的流程如下:
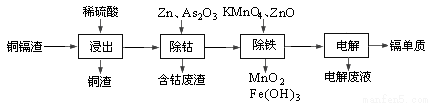
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol/L计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是__________________。
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3。该微电池的正极反应式为_____。
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
① 除铁过程中,理论上参加反应的物质n(KMnO4)∶n(Fe2+)=_________。
② 除铁时加入ZnO控制反应液pH的范围为________________。
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:_____________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是_____。
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:简答题
(18分)绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品的重要成分.如图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

查询资料,得有关物质的数据如下:
25℃时 | pH值 | 25℃时 | pH值 |
饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
(1)写出Fe和Fe2O3在硫酸溶液中发生反应的离子方程式为____、 ______ 、 __________;
(2)操作II中,通入硫化氢至饱和的目的是:①除去溶液中的Sn2+离子;②_________;③在溶液中用硫酸酸化至pH=2的目的是___________.
(3)操作IV的顺序依次为_____________、____________、过滤洗涤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②___________.
(5)常温下,Ksp[Fe(OH)2]=1.64×10-14,则求得反应:Fe2++2H2O Fe(OH)2+2H+的平衡常数为:_______________(保留1位小数);
Fe(OH)2+2H+的平衡常数为:_______________(保留1位小数);
查看答案和解析>>
科目:高中化学 来源:2017届山东省菏泽市高三上学期期末学分认定考试B卷化学试卷(解析版) 题型:选择题
在容积为2L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )

A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃时,该反应的平衡常数为25
C. 当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D. 由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com