
 2C(g),在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用C浓度的变化表示的该反应在这段时间内的平均反应速率为 .
2C(g),在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用C浓度的变化表示的该反应在这段时间内的平均反应速率为 . 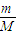 =
=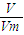 计算物质的量、质量关系;
计算物质的量、质量关系;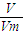 =
=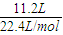 =0.5mol,乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了8.4g,即为乙烯的质量,所以乙烯的物质的量为n=
=0.5mol,乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了8.4g,即为乙烯的质量,所以乙烯的物质的量为n=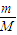 =
=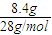 =0.3mol,则乙烷的物质的量为:0.5mol-0.3mol=0.2mol,质量为:0.2mol×30g/mol=6g,所以,乙烯与乙烷的质量之比为8.4g:6g=7:5,故答案为:7:5,
=0.3mol,则乙烷的物质的量为:0.5mol-0.3mol=0.2mol,质量为:0.2mol×30g/mol=6g,所以,乙烯与乙烷的质量之比为8.4g:6g=7:5,故答案为:7:5, =
= =0.04mol?L-1?s-1,而同一反应,不同物质反应速率速率之比等于计量数之比,所以v(C)=2 v(A)=2×0.04mol?L-1?s-1=0.08mol?L-1?s-1,故答案为:0.08mol/(L?s).
=0.04mol?L-1?s-1,而同一反应,不同物质反应速率速率之比等于计量数之比,所以v(C)=2 v(A)=2×0.04mol?L-1?s-1=0.08mol?L-1?s-1,故答案为:0.08mol/(L?s).

科目:高中化学 来源: 题型:
| 淀粉酶 |
| 淀粉酶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2C(g),在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用C浓度的变化表示的该反应在这段时间内的平均反应速率为
2C(g),在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用C浓度的变化表示的该反应在这段时间内的平均反应速率为查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)酿酒和造醋是古代劳动人民的智慧结晶,白酒和醋也是日常生活中常见的有机物。
(1)醋酸可用于除去水壶中的水垢,成份主要是CaCO3和Mg(OH) 2。写出醋酸与Mg(OH) 2反应的离子方程式_______________________。食盐中常加入KIO3来补碘,为验证食盐中的KIO3,可在食盐中加入醋酸,再加入KI和淀粉溶液。反应的离子方程式为____________________________。
(2)酿制米酒的过程中是米中的淀粉在酶的作用下生成葡萄糖。写出化学方程式_____________________________,然后葡萄糖在酶的作用下生成乙醇。
(3)在酿制米酒的过程中,有可能变酸,这里因为产生了醋酸。为了除去米酒中的酸味有人建议向米酒中加入红热的铅,使它与醋酸生成有甜味的醋酸铅。你认为此法是否可行_____(填行,不可行),原因是___________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年湖北省孝感高中高一下学期期末考试化学试题 题型:填空题
(9分)酿酒和造醋是古代劳动人民的智慧结晶,白酒和醋也是日常生活中常见的有机物。
(1)醋酸可用于除去水壶中的水垢,成份主要是CaCO3和Mg(OH) 2。写出醋酸与Mg(OH) 2反应的离子方程式_______________________。食盐中常加入KIO3来补碘,为验证食盐中的KIO3,可在食盐中加入醋酸,再加入KI和淀粉溶液。反应的离子方程式为____________________________。
(2)酿制米酒的过程中是米中的淀粉在酶的作用下生成葡萄糖。写出化学方程式_____________________________,然后葡萄糖在酶的作用下生成乙醇。
(3)在酿制米酒的过程中,有可能变酸,这里因为产生了醋酸。为了除去米酒中的酸味有人建议向米酒中加入红热的铅,使它与醋酸生成有甜味的醋酸铅。你认为此法是否可行_____(填行,不可行),原因是___________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年湖北省高一下学期期末考试化学试题 题型:填空题
(9分)酿酒和造醋是古代劳动人民的智慧结晶,白酒和醋也是日常生活中常见的有机物。
(1)醋酸可用于除去水壶中的水垢,成份主要是CaCO3和Mg(OH) 2。写出醋酸与Mg(OH) 2反应的离子方程式_______________________。食盐中常加入KIO3来补碘,为验证食盐中的KIO3,可在食盐中加入醋酸,再加入KI和淀粉溶液。反应的离子方程式为____________________________。
(2)酿制米酒的过程中是米中的淀粉在酶的作用下生成葡萄糖。写出化学方程式_____________________________,然后葡萄糖在酶的作用下生成乙醇。
(3)在酿制米酒的过程中,有可能变酸,这里因为产生了醋酸。为了除去米酒中的酸味有人建议向米酒中加入红热的铅,使它与醋酸生成有甜味的醋酸铅。你认为此法是否可行_____(填行,不可行),原因是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com