
下列各组离子,能在溶液中大量共存的是
A.H+、Al3+、Cl-、NO3- B.Al3+、Mg2+、SO42-、OH-
C.Fe2+、H+、K+、MnO4- D.Cu2+、H+、Cl-、HCO3-
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源:2015-2016学年江西省高一上第二次段考化学试卷(解析版) 题型:选择题
下列关于溶液和胶体的说法正确的是
A.可以利用电泳现象区分溶液和胶体
B.可以利用胶体的丁达尔效应区分溶液和胶体
C.可以用过滤的方法分离溶液和胶体
D.溶液呈电中性,胶体是带电的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津静海一中高一上12月学业调研化学卷(解析版) 题型:简答题
怎样用化学方法除去下列物质中混有的少量杂质,写出除杂需加入的试剂以及发生反应的离子方程式。
需加入的除杂试剂 | 发生反应的离子方程式 | |
①CO2气体中混有HCl杂质 | ||
②NaHCO3溶液中混有Na2CO3 | ||
③FeCl2溶液中混有FeCl3杂质 | ||
④Fe2O3固体中混有Al2O3杂质 |
学法题:归纳总结除杂试剂选择的方法
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期12月阶段测化学试卷(解析版) 题型:填空题
(1)2015年8月12日天津港危化品爆炸,教训极为深刻。其中化学品之一是氰化钠(NaCN):白色固体,可溶于水,剧毒,致死量50~250mg。氰化钠遇水或酸生成剧毒易燃的氰化氢(HCN)气体。处理氰化物可用碱性氯化法,该方法发生三步反应,写出其离子方程式。
①氯气与氢氧化钠溶液反应生成次氯酸盐(ClO-): 。
②次氯酸盐氧化氰化物(CN-)生成氰酸盐(CNO-):ClO-+CN-=CNO-+2Cl-
③过量的次氯酸盐氧化氰酸盐生成CO32-和N2: 。
(2) 用ClO2 处理泄漏的氰化钠(NaCN),得到无毒的NaCl、N2 和CO2。若处理含NaCN 4×10-5mol·L-1的废水 1000L,至少需要ClO2 的质量为___________g。
(3)化学是一门以实验为基础的科学,下列叙述正确的是______(填写序号).
①将0.2mol•L-1FeCl3溶液滴加到沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体.
②分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出。
③用NaOH固体配制100g 10%的氢氧化钠溶液时,用到的玻璃仪器主要有玻璃棒、烧杯、量筒和胶头滴管。
④托盘天平、容量瓶、量筒、滴定管等定量仪器均标有0刻度线。
⑤除去CO2中HCl,可将混合气体通过盛有饱和Na2CO3溶液的洗气瓶。
⑥纯净的氢气在氯气中安静地燃烧,产生苍白色火焰,瓶口伴有白雾。
⑦加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有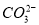 。
。
(4)化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
A.定性检验SO32-,可用HNO3酸化的BaCl2溶液
B. 配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度
C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液
D.检验氧化铁中的氧化亚铁,先用硫酸溶液溶解,然后加入盐酸酸化的高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:填空题
实验室常用NaOH溶液和氨水(NH3·H2O)两种碱溶液来制取不同的金属氢氧化物,请选择合适的试剂来制取以下的金属氢氧化物:
(1)要制取Fe(OH)3时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(2)要制取Fe(OH)2时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(3)要制取Cu(OH)2时,可用NaOH溶液与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
(4)要制取Al(OH)3时,可用氨水与__________(写化学式)反应,所得到的沉淀为________色,离子方程式为:____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
以下关于合金的说法不正确的是
A.合金的硬度往往大于它的纯金属
B.合金的熔点高于它的成分金属
C.青铜是我国使用最早的合金
D.钢是使用量最大,用途最广的合金
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:计算题
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积为2L的密闭容器中,发生如下反应:N2+ 3H2  2NH3。
2NH3。
(1)若反应进行5min时,测得n(N2) = 1.8mol,n(NH3) = 0.4mol。
计算:①a的值; ②用H2浓度的变化表示的反应速率。
(2)反应达平衡时,混合气体的总物质的量为5.0mol,其中NH3的含量(体积分数)为40%。
计算:上述温度下该反应的化学平衡常数。
查看答案和解析>>
科目:高中化学 来源:2015-2016年江西省高二上12月月考化学试卷(解析版) 题型:计算题
某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为180。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求该有机物的分子式。
查看答案和解析>>
科目:高中化学 来源:2015-2016年山东省高一上12月月考化学试卷(解析版) 题型:选择题
利用N2→NH3→NO→NO2→HNO3这一过程制备HNO3,有关上述各物质的叙述不正确的是
A.工业固氮的常用方法是N2和H2合成NH3
B.可利用Cu与硝酸的反应,将N元素转化为NO或NO2
C.为使上述各步骤依次发生,必须向每个步骤中提供氧化剂
D.实验室可利用氢氧化钙固体与NH4Cl固体混合加热制备NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com