
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。
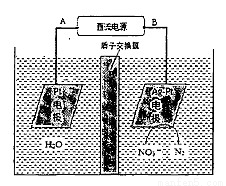
①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。
(1)①N≡N 2NO3-+5H2 N2+2OH-+4H2O 0.001mol/(L·min)
N2+2OH-+4H2O 0.001mol/(L·min)
③加酸,升高温度,加水
(2)A, 2NO3-+6H2O+10e-=N2+12OH- ②14.4
【解析】
试题分析:(1) ②废水不应显酸性(HNO3易挥发),而是中性或碱性,所以O2-在水中以H2O或OH-形式存在,有题意也可看出生成OH-(溶液pH由7变为12),依据氧化还原反应规律可配平:

pH=12 c(H+)=1×10-12mol·L-1
c(H+)=1×10-12mol·L-1
 c(OH-)=
c(OH-)=  1×10-2mol·L-1
1×10-2mol·L-1
υ(NO3-)=υ(OH-)= 1×10-10mol·L-1 /10min= 0.001mol·L-1·min-1
③由方程式知NO2-+H2O HNO2+OH- △H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
HNO2+OH- △H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
(2)①2 O3-+10e-→
O3-+10e-→ +6O2,所以B极为电源负极,A极为电源正极。
+6O2,所以B极为电源负极,A极为电源正极。
O2-+H2O=2OH-,可以写出阴极反应式:2NO3-+6H2O+10e- = N2↑+12OH-
② 左(+)阳极:4H2O(OH-)-4e-=4H++O2↑+2H2O
右(- )阴极:2NO3-+6H2O+10e- = N2↑+12OH-
10 e- O2(左)- 1N2(右)-10H+
O2(左)- 1N2(右)-10H+
10mol  mol 1mol 10mol
mol 1mol 10mol
2mol 0.5mol 0.2mol 2mol
由于阴阳极之间被质子交换膜隔开,左侧电解产生的H+会穿过质子交换膜进入右侧,所以:
△m左=m(O2)+m(H+)=0.5mol×32g·mol-1+2mol×1g·mol-1=18g
△m右= m(N2)-m(H+)=0.2mol×28g·mol-1-2mol×1g·mol-1=3.6g
△m左-△m右=18g-3.6g = 14.4g
考点:电解原理及相关计算。


科目:高中化学 来源:2015届山东省济宁市高二3月质检化学试卷(解析版) 题型:选择题
某甲酸溶液中含有甲醛,用下列方法可以证明的是
A.加入足量的新制氢氧化铜并加热煮沸,有砖红色的沉淀
B.加入过量的氢氧化钠充分反应后的溶液能发生银镜反应
C.将试液进行酯化反应后的混合液能发生银镜反应
D.加入足量氢氧化钠后,蒸馏出的气体通入新制的氢氧化铜悬浊液加热有砖红色沉淀
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
相同温度下等物质的量浓度的下列溶液中,pH值最大的是
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D.(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源:2015届天津市和平区高二上学期期末考试化学试卷(解析版) 题型:选择题
某同学按图所示的装置进行电解实验,下列说法错误的是( )。
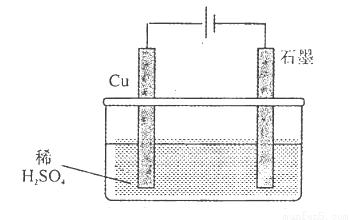
A.电解初期,石墨电极上有H2产生
B.整个电解过程中,H+的浓度不断增大
C.电解一定时间后,石墨电极上有铜析出
D.电解初期,总反应方程式为:
查看答案和解析>>
科目:高中化学 来源:2015届天津市南开区高二上学期期末考试化学试卷(解析版) 题型:选择题
已知温度T时,水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA溶液与b mol·L-1的一元碱BOH溶液等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= 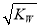 mol·L-1
mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源:2015届天津市南开区高二上学期期末考试化学试卷(解析版) 题型:选择题
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应说法正确的,下列是
A.弱酸溶液产生较多的氢气
B.强酸溶液产生较多的氢气
C.两者产生等量的氢气
D.无法比较两者产生氢气的量
查看答案和解析>>
科目:高中化学 来源:2015届天津市五区县高二上学期期末考试化学试卷(解析版) 题型:选择题
pH=2的两种一元酸X和Y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加0.1 mol/L NaOH至pH=7,消耗NaOH溶液的体积为Vx、Vy,下列说法正确的是
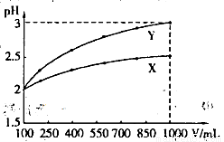
A.X为弱酸,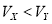 B.Y为强酸,
B.Y为强酸,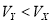
C.X为强酸,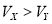 D.Y为弱酸,
D.Y为弱酸,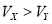
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高二3月月考化学试卷(解析版) 题型:计算题
3.24g淀粉和3.42g蔗糖混合,在一定条件下水解(假设完全水解),若得到ag葡萄糖和bg果糖,则a与b的比值是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com