
(14分)
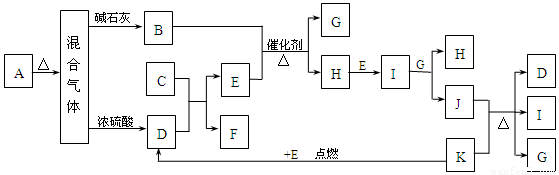
(1)下图中A~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体。已知A是一种不含金属元素的盐,受热分解能得到物质的量相等的三种产物;A加热后生成的混合气体若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体),若通过浓硫酸则只剩余气体D(D为无色无味气体);C为淡黄色固体。各物质间的转化关系如下图所示:
请回答下列问题:
①写出C的电子式: 。
②写出A的溶液与足量NaOH溶液反应的离子方程式:
。
③写出实验室制取B的化学方程式:
。
④写出J与K反应的化学方程:
。
(2)火星探测车在火星大气中检测到了气体M。资料显示,M分子是三原子分子,其相对分子质量为60,在地球环境下M易分解。粉末状的KSCN与95%的硫酸在一定条件下反应可得到气体M和两种硫酸氢盐,生成物的物质的量之比是1﹕1﹕1。则两种硫酸氢盐的化学式为 、 ,气体M的结构式是 。
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
非选择题 【共道小题,分】【14分】下图是实验室验证某铜银合金完全溶解于一定量的浓硝酸时,生成NO2气体中含有NO的实验装置。常温下,NO2与N2O4混合存在,在低于0 ℃时,几乎只有白色N2O4晶体存在。
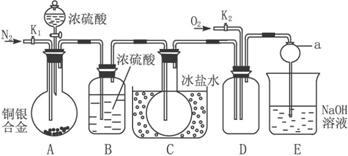
(1)反应前打开A部分的活塞K1,持续通一段时间氮气,其理由是_____________________
_____________________________________________________________________。
(2)若装置中缺B部分,其后果是__________________________________________________。
(3)反应结束后,打开D部分的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热的氧气,则瓶内气体的颜色比前者更深,其原因是__________________________。
(4)E部分中a仪器所起的作用是______________________________________________。
(5)已知该铜银合金的质量为15 g,加入40 mL 135 mol·L-1的浓硝酸,实验结束后,A部分烧瓶内溶液中的c(H+)=1 mol·L-1(假设反应中HNO3既无挥发也无分解,体积仍为40 mL)。
①参加反应硝酸的物质的量为_____________________。
②为测定铜银合金中铜的质量分数,还需要进行的主要实验操作是_____________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省高三10月月考化学试卷(解析版) 题型:填空题
(14分) (1) 2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如下图所示。
①请写出从C口通入O2发生的电极反应式___________________。
②以石墨电极电解饱和食盐水,电解开始后在______________的周围(填“阴极”或“阳极”)先出现红色。假设电池的理论效率为80%(电池的理论效率是指电池产生的最大电能与电池反应所释放的全部能量之比),若消耗6.4g甲醇气体,外电路通过的电子个数为__________________(保留两位有效数字)。

(2)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18mol2•L-2,Ksp(CuS)=1.3×10-36mol2•L-2。
请用离子方程式说明上述除杂的原理___________________________________________。
(3)工业上为了处理含有Cr2O72-的酸性工业废水, 用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为______________________________________________。
②常温下,Cr(OH)3的溶度积Ksp =1×10—32 mol4•L-4,溶液的pH至少为____,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78mg•L—1的废水,需用绿矾的质量为 kg。(保留主要计算过程)
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖南省名校高三9月第一次联考化学试卷(解析版) 题型:填空题
(每空2分,共14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:
① G是一种红棕色粉末、C既能与盐酸又能与NaOH溶液反应
② I是一种常见的温室气体,它和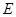 可以发生反应:2E+I
可以发生反应:2E+I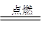 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
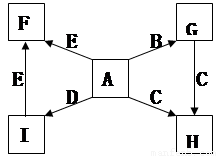
回答问题:
(1)写出G→H的化学方程式为________________________;
此反应在工业上常用于焊接钢轨,实验室在演示该实验时,在装置中加入G、C混合物后,引发此反应的操作是 ;
(2)化合物Ⅰ的电子式为______________________,
(3)用适量的盐酸溶解G后,所得溶液叫蚀铜剂,常用来洗涤印刷电路板上的铜,写出该反应的离子方程式为________________;
(4)E在I中燃烧观察到的现象是_______________________。
(5)在氩气的保护下,将一定计量的C、E加热熔炼可获得一种潜在的贮氢材料E17C12 ,该材料吸氢的反应方程式为E17C12+17H2 = 17EH2+12C
①熔炼制备贮氢材料E17C12时通入氩气的目的是
②1mol E17C12完全吸氢后,将得到的产物与足量的盐酸完全反应。释放出H2的物质的量为
查看答案和解析>>
科目:高中化学 来源:2010-2011学年重庆市七区2010-2011学年高三第一次调研测试(理综)化学试卷 题型:填空题
(14分)
(1)下图中A~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体。已知A是一种不含金属元素的盐,受热分解能得到物质的量相等的三种产物;A加热后生成的混合气体若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体),若通过浓硫酸则只剩余气体D(D为无色无味气体);C为淡黄色固体。各物质间的转化关系如下图所示:
请回答下列问题:
①写出C的电子式: 。
②写出A的溶液与足量NaOH溶液反应的离子方程式:
。
③写出实验室制取B的化学方程式:
。
④写出J与K反应的化学方程:
。
(2)火星探测车在火星大气中检测到了气体M。资料显示,M分子是三原子分子,其相对分子质量为60,在地球环境下M易分解。粉末状的KSCN与95%的硫酸在一定条件下反应可得到气体M和两种硫酸氢盐,生成物的物质的量之比是1﹕1﹕1。则两种硫酸氢盐的化学式为 、 ,气体M的结构式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com