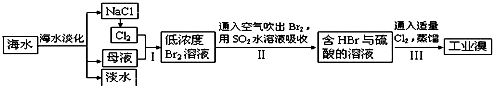
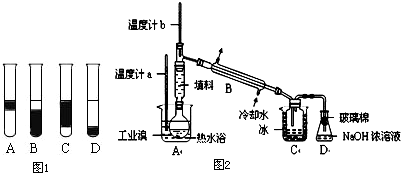
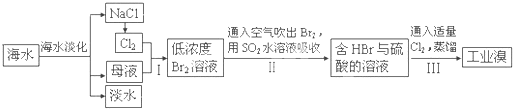
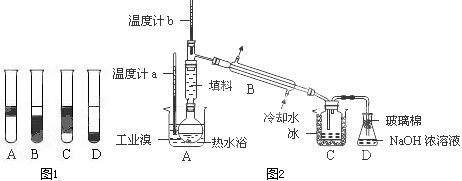
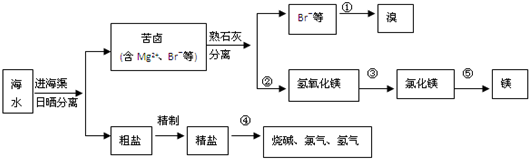
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
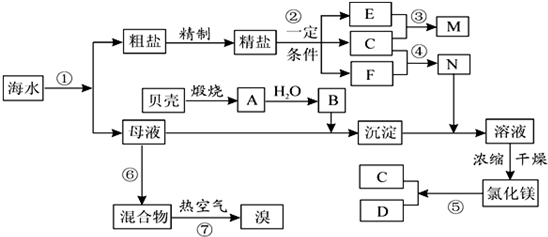
请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N
HCl
HCl
、B
石灰乳
石灰乳
.
(2)写出反应②的化学方程式
(3)写出反应③的离子方程式:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
,
Ⅱ粗盐中含有Ca
2+、Mg
2+、SO
42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
AD
AD
.
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br
2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是
C
C
.
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因:
.
(3)若用来提取Br
2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是
CD
CD
.
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有
挥发
挥发
性.
(4)母液用来提取Mg和Br
2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br
2乙:母液先提取Br
2,后提取Mg
请你判断哪个更合适?
乙
乙
(填“甲”或“乙”),理由是
若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
.




 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案