
【题目】CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下:
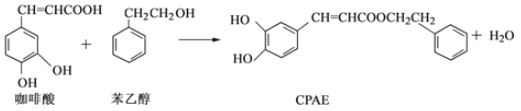
下列说法正确的是( )
A. 苯乙醇属于芳香醇,它与邻甲基苯酚互为同系物
B. 1molCPAE最多可与含3molNaOH的溶液发生反应
C. 用FeCl3溶液不可以检测上述反应中是否有CPAE生成
D. 咖啡酸、苯乙醇及CPAE都能发生取代、加成和消去反应
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对m g无水三草酸合铁酸钾(K3[Fe(C2O4)3]]受热分解产物进行探究,并对所得气体产物和固体产物进行验证(查阅资料得知:三草酸合铁酸钾热分解的气体产物中含有CO和CO2)。利用如图装置进行实验(夹持仪器已略去)。
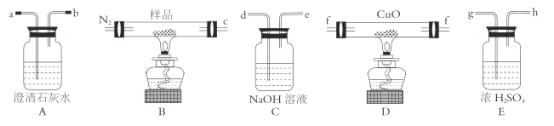
回答下列问题:
(1)按气流方向各装置依次连接的合理顺序为______;(填接口代号,装置可重复使用)
(2)反应开始前依次进行如下操作:组装仪器、_______、加药品、通氮气一段时间后点燃酒精灯。反应结束后的操作包括:①停止通氮气②熄灭酒精灯③冷却至室温。正确的顺序为___________________;
(3)通入氮气的目的是_____________________。
(4)实验中观察到第一个澄清石灰水变浑浊,则说明气体产物中有____________(写化学式)。能证明分解产物中有CO气体生成的实验现象是_________________。
(5)样品完全分解后,装置B中的残留物含有FeO和Fe2O3。
(6)测定三草酸合铁酸钾中铁的含量。
①将装置B中完全分解后的残留物置于锥形瓶中,溶解后加稀H2SO4酸化的x mol/LKMnO4溶液滴定至终点。滴定终点的现象是______。该过程发生反应的离子方程式为______。
②向上述溶液中加入过量KI-淀粉溶液,充分反应后,用y mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液V mL(已知I2+2S2O32-=2I-+S4O62-)。该晶体中铁的质量分数的表达式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的四种短周期元素。n、p、r是由这些元素组成的二元化合物。m 是元素W的单质。q是元素Y的单质且是制作太阳能电池的原料。p在常温下为常见无色液体,0.010mol·L-1的r溶液中c(H+)为0.010 mol·L-1,s是弱酸且不溶于水。上述物质的转化关系如图所示。下列说法不正确的是
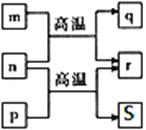
A.r易溶于p
B.原子半径:Z<Y
C.最高价氧化物对应水化物的酸性:Y<Z
D.最简单氢化物的稳定性:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
B. 甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-![]() HCOO-+NH4++2Ag↓+3NH3 +H2O
HCOO-+NH4++2Ag↓+3NH3 +H2O
C. 乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2 +OH-![]() Cu2O↓+CH3COO-+3H2O
Cu2O↓+CH3COO-+3H2O
D. 向小苏打溶液中加入醋酸:CO32-+2CH3CHOOH=CO2+H2O+2CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是一种难溶于水、密度为 1.46g/cm3、沸点为 38.4℃的无色液体。如图为实绘室制备溴乙烷的装置示意图(夹持仅器已略去)。 G 中盛蒸馏水,实验时选用的药品有:溴化钠、 95%乙醇、浓H2SO4。边反应边蒸馏,蒸出的溴乙烷用水下收集法获得。实验室制备溴乙烷的反应原理如下:NaBr+H2SO4(浓) ![]() NaHSO4+HBr CH3CH2OH+HBr→CH3CH2Br+H2O
NaHSO4+HBr CH3CH2OH+HBr→CH3CH2Br+H2O
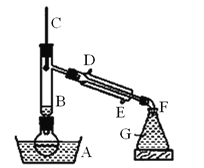
已知药品的用量:
①NaBr(s)0.5mol,②浓硫酸 65mL(98%、密度1.84g/cm3),③乙醇 0.35mol。
可能存在的副反应有:醇在浓硫酸存在下脱水生成烯和醚, Br-被浓硫酸氧化为 Br2等。
试问答:
(1)冷凝水从_______处充入,水浴加热的温度最好控制在______ ℃左右。
(2)为防止副反应的发生,向圆底烧瓶内加入药品时,还需加入适量的______。
(3)装置 B 的作用是:①使溴乙烷馏出,②_______________________________。
(4)采取边反应边蒸馏的主要原因是______________________________________。
(5)粗产品用水洗涤后有机层仍呈红棕色,欲除去该杂质,可加入的试剂为___ (填编号)。
a.碘化钾溶液 b.氢氧化钠溶液 c.亚硫酸氢钠溶液 d.饱和氯化钠溶液
(6)本实验的产率为 60%,则可制取溴乙烷______g。(保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
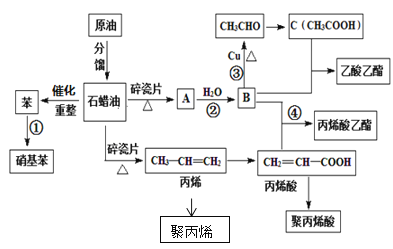
(1)A的结构简式为__,丙烯酸中官能团的名称为___。
(2)写出下列反应的反应类型①__,③___。
(3)用一种方法鉴别B和C,所用试剂是__。
(4)写出下列反应方程式:
丙烯→聚丙烯__;
丙烯酸+B→丙烯酸乙酯__。
查看答案和解析>>
科目:高中化学 来源: 题型:
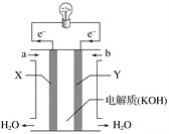
【题目】(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氢气从__口通入(填“a”或“b”),Y极为电池的___(填“正”或“负”)极。
(2)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Ag2O是__极,Zn发生__反应。
②电子由__极流向__极(填“Zn”或“Ag2O”),当电路通过0.1mol电子时,负极消耗物质的质量是___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com