
H(g)+H(g) = H2(g) ;△H = -435.7KJ/mol,这个式子说明的意义是
A、氢原子的能量比氢分子的能量低
B、一个氢原子与一个氢原子结合生成1个氢分子,且放出435.7KJ的能量
C、1mol氢分子分解成2mol氢原子要吸收435.7KJ能量
D、2mol氢原子结合成1mol氢分子要吸收435.7KJ能量
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 太阳光 |
| ||
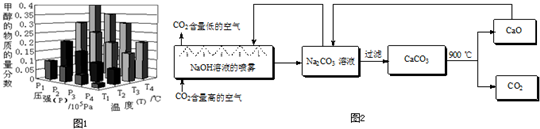
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:浙江省期中题 题型:填空题
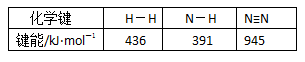
 2NH3(g) ;△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________(注明“+“-”)。
2NH3(g) ;△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________(注明“+“-”)。 CH3OH(g);△H =-90.8 kJ·mol-1
CH3OH(g);△H =-90.8 kJ·mol-1  CH3OCH3(g) + H2O(g);△H=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);△H=-23.5 kJ·mol-1  CO2(g) + H2(g);△H=-41.3 kJ·mol-1
CO2(g) + H2(g);△H=-41.3 kJ·mol-1  CH3OCH3(g) + CO2 (g)的△H=____________。
CH3OCH3(g) + CO2 (g)的△H=____________。查看答案和解析>>
科目:高中化学 来源: 题型:
(08浙江金丽衢十二校联考) N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是()
A.![]() N2H4(g)+
N2H4(g)+![]() O2(g)====
O2(g)====![]() N2(g)+H2O(g);ΔH=+267 kJ?mol-1
N2(g)+H2O(g);ΔH=+267 kJ?mol-1
B.N2H4(g)+O2(g)====N2(g)+2H2O(l);ΔH=-133.5 kJ?mol-1
C.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=+534 kJ?mol-1
D.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=-534 kJ?mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com