
 N和B元素及其化合物在工农生产中有很重要的应用.
N和B元素及其化合物在工农生产中有很重要的应用.分析 (1)根据N最外层有5个电子,写出价电子排布式;同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素的第一电离能大于其相邻元素;
(2)根据价层电子对互斥理论确定原子的杂化方式以及分子空间构型;
(3)原子晶体的硬度较大,为空间网状结构,原子晶体中含有共价键;
(4)利用均摊法确定该化合物的化学式.
解答 解:(1)因N最外层即第二层有5个电子,所以价电子排布式为:2s22p3; 同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素的第一电离能大于其相邻元素,所以三种元素的第一电离能由大到小的顺序为:N>O>B;
故答案为:2s22p3;N>O>B;
(2)NH3中N原子形成3个δ键和1个孤电子对,中心原子sp3杂化;BF3中B原子含有3个σ键且不含孤电子对,中心原子sp2杂化,所以BF3为平面三角形构型,
故答案为:sp3;平面三角形;
(3)BN的硬度较大,结构与金刚石相似,所以BN是原子晶体,根原子晶体中只含有共价键,所以微粒间存在的作用力是共价键,故答案为:原子;共价键;
(4)该晶胞中,B原子个数=6,Mg原子个数=2×$\frac{1}{2}$+12×$\frac{1}{6}$=3,所以Mg原子和B原子个数之比为6:3=2:1,所以其化学式为MgB2,故答案为:MgB2.
点评 本题考查了物质结构和性质,涉及化学键的判断、核外电子排布式的书写、晶胞的计算等知识点,注意(4)中顶点上的原子被6个晶胞共用而不是8个晶胞,为易错点.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径:F<Mg<K | B. | 稳定性:PH3>H2S>NH3 | ||
| C. | 酸性:H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3<Mg(OH)2<KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
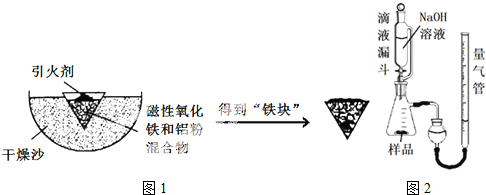
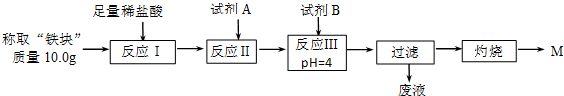
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酸性:H2SO4>HClO4>HBrO4 | B. | 碱性:RbOH>KOH>NaOH | ||
| C. | 非金属性:P>S>Cl | D. | 气态氢化物稳定性:HF>HCl>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3(CH2)4CH3 1,4-二甲基丁烷 | |
| B. | CH3CH(CH3)CH=CH2 甲基丁烯 | |
| C. | CH3CH2CH(CH3) CH2OH 2-甲基-1-丁醇 | |
| D. | CH2ClCH2Cl 二氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com