
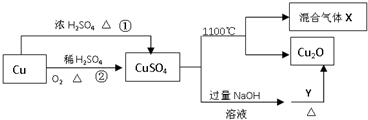
| A. | 途径①和途径②都体现了硫酸的酸性和氧化性 | |
| B. | Y可以是酒精溶液 | |
| C. | CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 | |
| D. | 将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 |
分析 A.根据反应物和生成物的化学式判断,途径①产生二氧化硫气体表现浓硫酸强氧化性和酸性,途径②是表现硫酸的酸性,无强氧化性表现;
B、硫酸铜与氢氧化钠生成氢氧化铜沉淀,与Y生成氧化亚铜,知Y可为葡萄糖,因葡萄糖中有醛基;
C.硫酸铜分解生成Cu2O与氧气、SO2、SO3,依据电子守恒分析;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体.
解答 解:A.转化关系分析可知,途径①产生二氧化硫气体表现浓硫酸强氧化性和酸性,途径②是表现硫酸的酸性,无强氧化性表现,故A错误;
B.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,蔗糖是非还原性糖不能和氢氧化铁反应生成氧化亚铜,故B错误;
C. 硫酸铜分解生成Cu2O与氧气、SO3、SO2,根据2CuSO4═Cu2O+SO2↑+SO3↑+O2↑知,X可能是O2、SO2和SO3的混合气体,若只是二氧化硫和三氧化硫,铜元素、氧元素化合价只有降低,无元素化合价升高,故C错误;
D.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体,故D正确;
故选D.
点评 本题考查了物质的制备,解题的关键是掌握物质的性质,解答时要依据题干提供信息,结合相关知识细心分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ①④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发使用的主要仪器是蒸发皿、酒精灯、玻璃棒、带铁圈的铁架台 | |
| B. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 | |
| C. | 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 | |
| D. | 用规格为10 mL的量筒量取6.20 mL的液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溴乙烷与NaOH水溶液混合加热 | |
| B. | 甲醇与浓硫酸混合加热 | |
| C. | 乙醇与浓硫酸混合加热 | |
| D. | 2-溴丁烷与NaOH的乙醇溶液混合加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A+X-n | B. | A-X-n | C. | A+X+n | D. | A-X+n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol 甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5mol 1,3-丁二烯分子中含有 数为NA 数为NA | |
| D. | 1mol碳正离子(CH${\;}_{3}^{+}$)所含的电子总数为8NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com