
【题目】根据题给要求填空
(1)某元素的基态原子最外层电子排布式为3s23p2,它的次外层上电子云形状有________种,原子中所有电子占有________个轨道,核外共有________种运动状态不同的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_______。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________,F2-的电子排布式是______。
(4)M能层上有________个能级,有________个轨道,作为内层最多可容纳________个电子,作为最外层时,最多可含有________个未成对电子。
【答案】2 8 14 ![]() 13 1s22s22p6 3 9 18 3
13 1s22s22p6 3 9 18 3
【解析】
(1)某元素的基态原子最外层电子排布为3s23p2,该元素为Si,核外电子排布式为1s22s22p63s23p2,次外层能级为2s、2p,有s、p两种不同的轨道,电子云形状有2种。原子中所有电子占有8个轨道,分别为1s、2s、3s共3个轨道,3个2p轨道,2个3p轨道;原子核外有14个电子,每个电子的运动状态都不一样,因此有14种不同的运动状态;
(2)E原子核外占有9个轨道,且具有1个未成对电子,则其核外电子排布图为![]() ,从图可知,该原子为Cl原子,得到1个电子,形成Cl-,其结构示意图为
,从图可知,该原子为Cl原子,得到1个电子,形成Cl-,其结构示意图为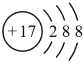 ;
;
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,F为短周期元素,能够形成离子F2-,只能是O2-或S2-,但是G也是短周期元素,G3+的电子层结构与F2-相同,如果F是S元素,则G不是短周期元素,因此F为O,G为Al;G为Al,其原子序数为13;F2-是O2-,其电子排布式1s22s22p6;
(4)M能层上3个能级,分别为3s、3p、3d;3s有1个轨道,3p有3个轨道,3d有5个轨道,共9个轨道;每个轨道可以容纳2个电子,作为内层最多可容纳9×2=18个电子;作为最外层时,只有3s、3p能级上填充电子,未成对电子最多,则3个3p轨道上均只有1个电子,最多可含有3个未成对电子。


科目:高中化学 来源: 题型:
【题目】根据《化学反应原理》中相关知识,按要求作答。
氯的单质、化合物与人类生产、生活和科研密切相关。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式: H2(g)+Cl2(g)=2HCl(g)△H = -184.6 kJ . mol-1,判断该反应属于_____(填“吸热”或“放热")反应。
(2)盐酸是一种强酸,补充完整电离方程式:HCl=___+Cl- 。室温下,将大小相等的镁条和铁片投入同浓度的稀盐酸中,产生氢气的速率较大的是________。
(3)84消毒液在防控新冠肺炎疫情中被大量使用,它是利用氯气与氢氧化钠溶液反应制成的.反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
①该反应____(填“是”或“不是”)氧化还原反应。
②室温下,84消毒液呈碱性,其pH___7 (填“>”或“<”)。
③84消毒液的有效成分NaClO,水解的离子方程式:ClO-+H2O=HClO+OH-,生成物中__具有很强的氧化性,可以使病毒和细菌失去生理活性;水解是吸热反应,升高温度平衡向_____(填“正反应”或“逆反应”)方向移动。
(4)电解熔融氯化钠可制取金属钠和氯气,装置如图所示(电极不参与反应):
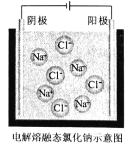
通电时,Na+向______(填“阳极”或“阴极")移动,写出生成金属钠的电极反应式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】轻质氧化镁和硼酸(H3BO3)都是重要的化工原料,可采用硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸和轻质氧化镁,其工艺流程如图:
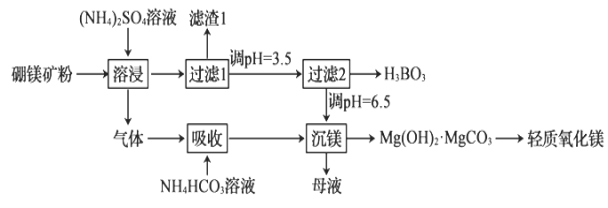
下列叙述错误的是( )
A.Fe2O3、Al2O3都不能溶于(NH4)2SO4溶液
B.进入“吸收”工序中的气体为NH3
C.若“过滤2”时调节溶液的碱性越强得到的硼酸越多
D.“沉镁”中得到的母液经加热后可返回“溶浸”工序循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断下列有关说法正确的是( )
A.羰基硫属于非极性分子B.羰基硫的电子式为![]()
C.羰基硫的沸点比CO2低D.羰基硫分子中三个原子处于同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用索氏提取器,用石油醚做溶剂从花生仁中提取油脂,装置如图。石油醚的主要成分为戊烷和已烷的混合物,沸程为:30℃~60℃。下列说法错误的是
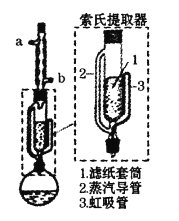
A.石油醚易挥发易燃烧,提取过程不可选用明火直接加热
B.石油醚的沸程较大,加热前不必加入沸石
C.烧瓶中的石油醚受热经侧管进入冷凝管,冷却后进入滤纸套筒与碎花生接触进行萃取
D.索氏提取器使用溶剂少,可循环连续萃取,萃取效率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性电池具有容量大、放电电流大的特点因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解质溶液,电池总反应式为:Zn+2MnO2+H2O=Zn(OH)2+Mn2O3。下列说法正确的是( )
A.电池工作时,锌是正极
B.电子由Zn电极通过外电路流向MnO2电极
C. MnO2电极发生氧化反应
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为原子序数依次减小的短周期主族元素,已知W、Y、Z的最外层电子数之和等于X的最外层电子数;由四种元素形成某化合物的结构如图所示。下列叙述不正确的是( )
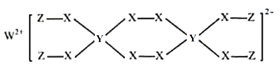
A.简单氢化物的稳定性:X>YB.简单离子半径:X>W
C.Y的最高价氧化物对应水化物为弱酸D.该化合物中各元素均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图进行实验,探究H2O2的分解反应。
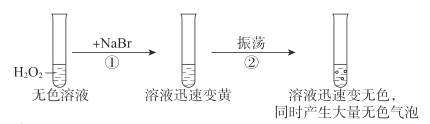
下列说法不正确的是( )
A.NaBr中的Br-加快了H2O2分解速率
B.双氧水既发生了氧化反应,又发生了还原反应
C.反应②的离子方程式是Br2+H2O2=2Br-+2H++O2↑
D.1molH2O2发生分解反应时,转移电子的物质的量是2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置中,A是氯气发生仪器,C、D为气体净化装置(C中装有饱和食盐水,D中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G中装有氢氧化钠溶液。
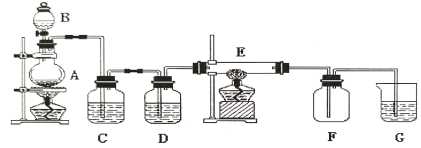
请回答下列问题:
(1)仪器A的名称是_________;B中盛装的药品是_____________;
(2)将实验室制氯气的化学方程式补充完整:MnO2+4HCl(浓)![]() ________ + Cl2↑+ 2H2O;
________ + Cl2↑+ 2H2O;
(3)C装置的作用是____________;D装置的作用是____________;
(4)E中发生化学反应的方程式为__________________;
(5)烧杯G中氢氧化钠溶液的作用是_______________;其发生反应的化学方程式为:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com