
计算题
2.4g的镁粉在100mL稀硫酸中完全溶解(反应前后溶液体积的变化忽略不计)。
(1)写出反应的离子方程式,并标出电子转移的方向和数目。
(2)求产生的气体在标准状况下的体积。
(3)求反应完全后所得溶液中镁离子的物质的量浓度。
科目:高中化学 来源:2016-2017学年山西太原五中高二12月阶段测文化学卷(解析版) 题型:选择题
埋在地下的输油铁管道,在下列情况下,被腐蚀速率最慢的是
A.在含铁元 素较多的酸性土壤 B.在潮湿疏松透气的土壤
素较多的酸性土壤 B.在潮湿疏松透气的土壤
C.在干燥致密不透气的土壤 D.在含碳颗粒较多,潮湿透气的中性土壤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高一上月考二化学卷(解析版) 题型:选择题
下列物质中,属于电解质但 不能导电的是( )
不能导电的是( )
A.四氯化碳 B.熔融的氯化铝 C.液态氯化钠 D.石墨
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高二上月考二化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
①0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO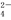
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-、NO3-
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-
A.②④⑥ B.②⑥ C.② D .①③⑤
.①③⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高二上月考二化学卷(解析版) 题型:选择题
甲酸的下列性质中,可以证明它是弱电解质的是
A.甲酸以任意比与水互溶
B.0.1mol/L甲酸溶液的c(H+)=10-3mol/L
C.10mL 1mol/L甲酸恰好与10mL  1mol/L NaOH溶液完全反应
1mol/L NaOH溶液完全反应
D.甲酸溶液的导电性比一元强酸溶液的弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:填空题
填空题
现有下列物质:①碳酸氢钠 ②氧化钠 ③SO2 ④铁 ⑤氧气 ⑥氢氧化钙 ⑦硫酸(H2SO4) ⑧乙醇 请将上述物质按下列要求分类,并将其序号填入空白处:
(1)按组成分类,属于单质的是__________,属于酸性氧化物的是__________,属于碱性氧化物的是__________;属于酸的是__________,属于碱的是__________,属于盐的是__________。
(2)按是否是电解质分类,属于电解质的是__________,属于非电解质的是__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:选择题
下列可以大量共存且溶液是无色的离子组是( )。
A.H+、Na+、NO3-、Cu2+ B.Ba2+、Mg2+、Cl-、SO42-
C.H+、K+、OH-、NO3- D.NO3-、SO42-、K+、Mg2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:推断题
某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种阳离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是________。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是_______,离子反应方程式为 。
(3)取(2)的滤液加入过量NaOH,出现白色沉淀,说明原溶液中肯定存在的离子有 。
(4)原溶液中可能大量存在的阴离子是下列A~D中的(填序号)________。
A.Cl- B.NO3- C.CO3 2- D.OH-
2- D.OH-
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:实验题
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
②牙膏中其它成分遇到盐酸时无气体产生。
实验内容:Ⅰ.摩擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤,往滤渣中加入过量NaOH溶液。
(1)该过程涉及主要反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的沉淀质量,以确定碳酸钙的质量分数。
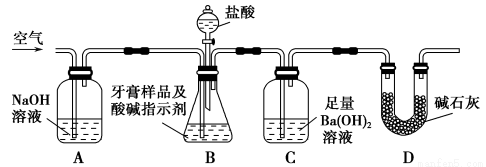
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________。
(3)C中反应生成沉淀的化学方程式是_____________________。
(4)下列各项措施中,能提高测定准确度的是________(填标号)。
a.滴加盐酸不宜过快
b.在A~B之间增添盛有浓硫酸的洗气装置
c.在加入盐酸之前,应排净装置内的CO2气体
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00 g样品三份,进行三次测定,测得C中产生沉淀平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(6)有人认为只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com